Перейти к:
Клинический случай хирургического лечения рецидивной формы пролапса тазовых органов у женщины репродуктивного возраста комбинированным методом с применением клеточных технологий
https://doi.org/10.69964/BMCC-2026-3-1-99-107
Аннотация
Введение. Пролапс тазовых органов остается одной из наиболее значимых проблем современной гинекологии, оказывая существенное влияние на качество жизни пациенток. Выбор хирургической тактики у женщин молодого возраста представляет особую сложность в связи с их репродуктивными планами и ограничениями в использовании синтетических имплантатов из-за риска mesh-ассоциированных осложнений, тогда как пластика собственными тканями, оставаясь базовым методом, сопряжена со значительным риском рецидива, особенно у пациенток с исходной несостоятельностью соединительной ткани. В этой связи актуальным является поиск биологически ориентированных органосохраняющих методов хирургического лечения, направленных не только на механическую коррекцию, но и на восстановление качества собственных тканей тазового дна.
Цель исследования. Представить клинический случай хирургического лечения рецидивной формы пролапса тазовых органов III стадии по классификации POP-Q у женщины репродуктивного возраста в объеме пластики собственными тканями в сочетании с подфасциальным введением микрофрагментированной адипозной ткани.
Материалы и методы. Нами проведено лечение и клиническое наблюдение за женщиной репродуктивного возраста, у которой диагностирована рецидивная форма пролапса тазовых органов III стадии по классификации POP-Q с преимущественным вовлечением переднего компартмента. Женщине проведено органосохраняющее хирургическое лечение в объеме пластики передней стенки влагалища собственными тканями в сочетании с подфасциальным введением микрофрагментированной адипозной ткани.
Результаты. При контрольном обследовании через 1, 3, 6 и 12 месяцев продемонстрировано восстановление анатомических соотношений органов малого таза: положение передней стенки влагалища соответствовало 0 стадии пролапса по системе POP-Q. Пациентка отметила значительное улучшение качества жизни, исчезновение ощущения пролабирования во влагалище, отсутствие дизурических симптомов и восстановление сексуальной функции.
Заключение. Установлена клиническая эффективность и безопасность комбинироваванного метода лечения рецидивной формой пролапса тазовых органов у пациентки репродуктивного возраста в объеме пластики собственными тканями в сочетании с подфасциальным введением микрофрагментированной адипозной ткани. Метод обеспечил восстановление анатомической поддержки переднего компартмента без признаков рецидива в течение 12 месяцев наблюдения, способствовал регрессу симптомов и улучшению качества жизни.
Ключевые слова
Для цитирования:
Лазукина М.В., Михельсон А.А. Клинический случай хирургического лечения рецидивной формы пролапса тазовых органов у женщины репродуктивного возраста комбинированным методом с применением клеточных технологий. Вестник охраны материнства и младенчества. 2026;3(1):99-107. https://doi.org/10.69964/BMCC-2026-3-1-99-107
For citation:
Lazukina M.V., Mikhelson A.A. Clinical case of surgical management of recurrent pelvic organ prolapse in a woman of reproductive age using a combined approach with cell-based technologies. Bulletin of maternal and child care. 2026;3(1):99-107. (In Russ.) https://doi.org/10.69964/BMCC-2026-3-1-99-107
Введение
Пролапс тазовых органов (ПТО) представляет собой одно из наиболее распространённых хронических заболеваний в гинекологии, характеризующееся смещением органов малого таза вследствие несостоятельности связочно-фасциального и мышечного аппарата тазового дна. Современные эпидемиологические данные показывают, что после хирургического вмешательства по поводу ПТО частота рецидивов остаётся значительной, достигая в некоторых исследованиях 39 % случаев в отдаленные сроки после операции [1–3]. Возникновение рецидивных форм обусловлено индивидуальными факторами риска, включая объем и технические аспекты предшествующей операции, стадию заболевания, одновременное поражение нескольких компартментов, семейный анамнез, а также возраст на момент вмешательства по поводу первичного ПТО [4–9].
Хирургическое лечение ПТО у женщин репродуктивного возраста имеет принципиальные особенности. С одной стороны, необходимо обеспечить надёжную анатомическую коррекцию и минимизировать риск рецидива, с другой — сохранить репродуктивный потенциал и избежать применения синтетических имплантатов, использование которых сопряжено с риском развития имплантат-ассоциированных осложнений [10][11]. Крупные рандомизированные исследования показали, что хотя сетчатые системы могут снижать риск анатомического рецидива переднего компартмента, они сопровождаются более высокой частотой специфических осложнений и повторных вмешательств по поводу экспозиции имплантата [12]. Также известно, что повторные операции сопровождаются техническими трудностями, более высоким риском осложнений и ухудшением функциональных результатов, что обусловливает необходимость поиска новых стратегий хирургического лечения.
Таким образом в клинической практике вновь усилился интерес к нативной пластике собственными тканями. Однако систематические обзоры свидетельствуют о том, что изолированная передняя кольпоррафия ассоциирована с высокой частотой анатомических рецидивов, особенно при наличии исходной фасциальной несостоятельности [12][13]. Таким образом, перед современной реконструктивной гинекологией стоит задача разработки биологически ориентированных методов, сочетающих органосохраняющий подход с усилением регенеративного потенциала тканей тазового дна.
В последние десятилетия активно развивается направление регенеративной медицины, основанное на использовании клеточных технологий. Мезенхимальные стромальные клетки, в том числе полученные из жировой ткани, обладают способностью к паракринной регуляции воспаления, стимуляции ангиогенеза и ремоделированию внеклеточного матрикса [14]. Жировая ткань рассматривается как доступный и безопасный источник клеточного материала, а методы минимальной обработки позволяют получать микрофрагментированную адипозную ткань (МФАТ), содержащую клеточные и сосудистые компоненты стромально-васкулярной фракции [15].
Экспериментальные исследования продемонстрировали, что трансплантация адипозных стромальных клеток способствует восстановлению структуры фасциальных и мышечных элементов тазового дна, улучшает коллагеновый профиль и повышает механическую прочность тканей [16]. В клинической практике наибольшее распространение клеточные технологии получили при лечении стрессового недержания мочи. Систематический обзор клинических исследований показал, что инъекции аутологичных стволовых клеток могут приводить к уменьшению симптомов недержания и улучшению уродинамических показателей при удовлетворительном профиле безопасности [17].
В России исследования в области применения аутологичных клеточных технологий при дисфункциях тазового дна проводятся в рамках клинических и экспериментальных проектов, посвящённых использованию стромально-васкулярной фракции и адипозных клеток для коррекции стрессового недержания мочи и недостаточности сфинктерного аппарата [18][19]. Публикации отечественных авторов подтверждают регенеративный потенциал жировой ткани и её перспективность в реконструктивной урогинекологии, однако опыт применения МФАТ при пролапсе тазовых органов остаётся ограниченным [20].
В международной практике описаны пилотные клинические исследования и серии наблюдений, в которых аутологичная жировая ткань или стромально-васкулярная фракция использовались для биологического усиления зон реконструкции тазового дна, а также при коррекции стрессового недержания мочи [21][22]. Несмотря на ограниченный объём клинических исследований, имеющиеся экспериментальные и пилотные клинические данные указывают на перспективность применения клеточных технологий в реконструктивной хирургии тазового дна. Продемонстрировано их потенциальное влияние на модуляцию воспалительной реакции, стимуляцию ангиогенеза, активацию процессов ремоделирования внеклеточного матрикса в зоне реконструкции, что может способствовать формированию более стабильного и функционально состоятельного рубца.
Таким образом, сочетание нативной реконструкции с подфасциальным введением микрофрагментированной адипозной ткани представляет собой концептуально новый биологически ориентированный подход к лечению рецидивных форм ПТО. Он направлен не только на механическое восстановление анатомии, но и на качественное улучшение тканевых характеристик, что особенно актуально у женщин репродуктивного возраста с признаками дисплазии соединительной ткани и высоким риском рецидива ПТО.
Представленный клинический случай отражает возможность применения комбинированной органосохраняющей методики при рецидивном пролапсе III стадии у пациентки репродуктивного возраста и иллюстрирует перспективность интеграции технологий регенеративной медицины в реконструктивную хирургию тазового дна.
Цель исследования. Представить клинический случай хирургического лечения рецидивной формы пролапса тазовых органов III стадии по классификации POP-Q у женщины репродуктивного возраста в объеме пластики собственными тканями в сочетании с подфасциальным введением микрофрагментированной адипозной ткани.
Клиническое наблюдение
Представляем клиническое наблюдение пациентки с рецидивной формой пролапсом тазовых органов III стадии по классификации POP-Q, которой выполнено комбинированное хирургическое лечение в объеме пластики собственными тканями с подфасциальным введением микрофрагментированной адипозной ткани в соответствии с описанной методикой.
Амбулаторный этап. Пациентка К., 42 лет, обратилась в гинекологическое отделение ФГБУ НИИ ОММ МЗ РФ с жалобами на ощущение инородного тела во влагалище, чувство давления и тяжести в промежности, усиливающееся к концу дня и при физической нагрузке, дискомфорт при половом акте, частые позывы к мочесипусканию. В анамнезе у женщины одни роды через естественные родовые пути, плод массой 3850 г., послеродовый период без особенностей. Пациентка отмечает прогрессирование симптомов генитального пролапса спустя 6 месяцев после перенесенной передней кольпоррафии по поводу цистоцеле II стадия по POP-Q.С целью выявления признаков системной дисплазии соединительной ткани пациентке проведена фенотипическая оценка по шкале Кадуриной Т.И., включающей анализ соматических, кожных, сосудистых, суставных и висцеральных признаков. При объективном обследовании у пациентки выявлены следующие клинико-фенотипические маркеры: гипермобильность суставов: по тестам пассивного переразгибания мелких суставов кистей и локтевых суставов отмечена умеренная гипермобильность (переразгибание более 10 градусов) — 2 балла; плоскостопие продольное I–II степени — 1 балл; варикозное расширение вен нижних конечностей без трофических нарушений — 1 балл; сколиотическая деформация грудного отдела позвоночника I степени — 1 балл;тонкая, растяжимая кожа с наличием единичных стрий на передней брюшной стенке вне беременности — 2 балла;астенический тип телосложения (индекс массы тела 27 кг/м², однако с узкой грудной клеткой и относительным удлинением конечностей) — 1 балл.; раннее формирование пролапса тазовых органов при отсутствии выраженных акушерских травм — 2 балла как висцеральный маркер слабости соединительной ткани.
Суммарный показатель по шкале Кадуриной Т.И. составил 10 баллов, что в соответствии с диагностическими критериями (до 5 баллов — отсутствие или минимальные фенотипические признаки, 6–9 баллов — умеренные проявления, 10 баллов и более — клинически значимая дисплазия соединительной ткани) свидетельствует о наличии у пациентки клинически выраженной дисплазии соединительной ткани.
При гинекологическом осмотре выявлено цистоцеле III стадии по классификации POP-Q. При измерении стандартных точек, обозначающих положение и размеры структур тазового дна, для определения выраженности опущения, согласно системе POP-Q, получены следующие данные: Aa +2, Ba +2, C -3, gh 1, pb 3, tvl 10, Ap-3, Bp -3, D –3. Кашлевая проба и проба Вальсальвы отрицательные.
Стандартный гинекологический осмотр был дополнен измерением силы сокращений мышц тазового дна с помощью вагинальной пальпации с количественной оценкой по шкале Оксфорда, а также манометрическим исследованием с использованием цифрового перинеометра с пневматическим вагинальным эспандер-датчиком с технологией биологической обратной связи.
Сила мышц тазового дна оценена в 0 баллов по шкале Оксфорда как отсутствие различимых сокращений. При проведении манометрии замер силы мышечных сокращений оценивался трижды: при максимальном напряжении мышц тазового дна в течение 10 секунд с последующим интервалом расслабления 10 секунд. При 1 подходе давление воздуха в вагинальном датчике составило 65 mmHb, 2 подходе — 56 mmHb, 3 подходе — 51 mmHb. Максимальное время удержания сокращения мышц тазового дна составило 10 с при среднем давлении воздуха в датчике 53 mmHb.
Согласно действующим клиническим рекомендациям «Выпадение женских половых органов» (2024), пациенткам с пролапсом тазовых органов при наличии жалоб на ургентное недержание мочи или затруднённое мочеиспускание рекомендуется проведение инвазивного уродинамического исследования. Учитывая, что у данной пациентки отмечались жалобы на частые позывы к мочеиспусканию, выполнение комплексного уродинамического исследования (КУДИ) являлось клинически обоснованным. Для оценки состояния и функционирования нижних отделов мочевыводящей системы выполнено КУДИ, включавшее цистометрию, профилометрию, урофлоуметрию. Произведено капельное наполнение мочевого пузыря стерильным раствором. В ходе исследования отмечалась нормальная чувствительность мочевого пузыря, функция детрузора без нарушений, по данным профилометрии, функциональная длина уретры и давление в области наружного сфинктера в пределах нормы. Однако, по результатам урофлоуметрии, зафиксировано снижение максимального и среднего потока мочи — 10,5 и 4,5 мл/с соответственно. За счет этого увеличено время опорожнения мочевого пузыря — 182 с. Объем остаточной мочи составил 180 мл.
После комплексного клинико-лабораторного и инструментального обследования пациентке рекомендовано хирургическое лечение.
Наличие диспластического фенотипа рассматривается как фактор риска развития ПТО, раннего дебюта заболевания и повышенной вероятности рецидива после нативной реконструкции. Учитывая рецидив ПТО после нативной пластики и категорический отказ пациентки использовать синтетические имплантаты, определена тактика органосохраняющего хирургического лечения с применением собственных тканей в сочетании с подфасциальным введением микрофрагментированной адипозной ткани.
Стационарный этап. С целью проведения хирургического лечения ПТО пациентка госпитализирована в гинекологическое отделение ФГБУ «Уральский НИИ ОММ».
Хирургическое лечение выполнено под эндотрахеальным наркозом в 2 этапа (рисунок). 1 этап забор и заготовка аутологичного биоматериала. На первом этапе произведена малоинвазивная липоаспирация подкожно-жировой клетчатки передней брюшной стенки после инфильтрации раствором Кляйна. Получено около 25 мл липоаспирата. Материал обработан в закрытой стерильной системе путем механической микрофрагментации и промывания физиологическим раствором без применения ферментативной обработки и центрифугирования. В результате получено 8 мл микрофрагментированной адипозной ткани. 2 этап хирургической реконструкции тазового дна. На втором этапе выполнена комбинированная реконструктивная операция. Произведена гидропрепаровка передней стенки влагалища, срединный разрез слизистой, диссекция паравагинальных тканей, мобилизация и дупликатура пубоцервикальной фасции непрерывным швом рассасывающимся полимером. Контроль целостности мочевого пузыря — без особенностей. После завершения фасциального этапа, до ушивания слизистой оболочки, подготовленная МФАТ в объеме 8 мл равномерно введена в подфасциальное пространство вдоль линии шва передней стенки влагалища с формированием биологического матрикса в зоне реконструкции. Далее слизистая оболочка влагалища ушита отдельными рассасывающимися швами.
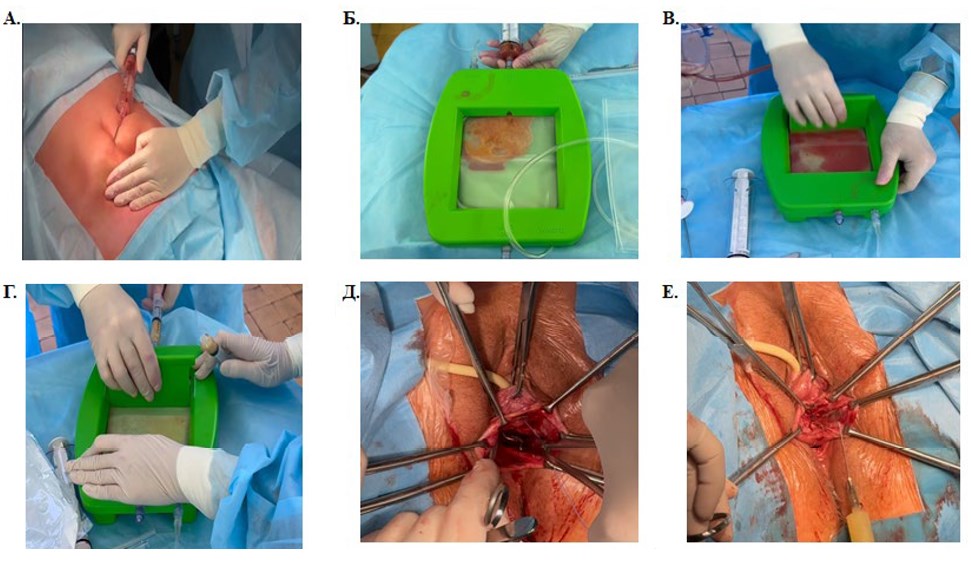
Рисунок. Хирургическая реконструкция тазового дна в объеме пластики собственными тканями в сочетании с подфасциальным введением микрофрагментированной адипозной ткани. А. Этап забора аутологичного биоматериала — липоаспирация веерообразными движениями. Б. Этап заготовки аутологичного биоматериала — введение липоаспирата и проведение его через микрофрагментационные панели с помощью шпателя. В. Этап заготовки аутологичного биоматериала – микрофрагментация и очищение липоаспирата от крови и липидных капель. Г. Этап заготовки аутологичного биоматериала — забор готовой микрофрагментированной адипозной ткани. Д. Этап хирургической реконструкции тазового дна – пластика пубоцервикальной фасции. Е. Этап хирургической реконструкции тазового дна — введение заготовленной аутологичной микрофрагментированной адипозной ткани в подфасциальное пространство.
Figure. Surgical reconstruction of the pelvic floor using native tissue repair combined with subfascial injection of micro-fragmented adipose tissue. A. Stage of autologous biomaterial harvesting — lipoaspiration using fanning movements. B. Stage of autologous biomaterial preparation — introduction of the lipoaspirate and its passage through microfragmentation screens using a spatula. C. Stage of autologous biomaterial preparation — microfragmentation and purification of the lipoaspirate from blood and lipid droplets. D. Stage of autologous biomaterial preparation – collection of the prepared micro-fragmented adipose tissue. E. Stage of surgical pelvic floor reconstruction – plication of the pubocervical fascia. F. Stage of surgical pelvic floor reconstruction – injection of the prepared autologous micro-fragmented adipose tissue into the subfascial space.
Продолжительность операции составила 45 минут. Интраоперационная кровопотеря — 50 мл. Послеоперационный период протекал без осложнений. Пациентка активизирована в первые сутки, выписана на 4-е сутки в удовлетворительном состоянии. При динамическом наблюдении через 1 месяц после операции пациентка жалоб на ощущение инородного тела во влагалище не предъявляла. Также пациентка отметила исчезновение дизурических симптомов. При осмотре признаков пролапса не выявлено, анатомическая поддержка переднего компартмента сохранена. Рана зажила первичным натяжением, рубец на передней стенке влагалища без особенностей. Через 6 месяцев отмечено стабильное анатомическое положение органов малого таза, отсутствие признаков рецидива. Пациентка возобновила половую жизнь, отметила исчезновение диспареунии и улучшение качества жизни. Объективно — слизистая влагалища розовая, эластичная, без участков инфильтрации и грубой рубцовой деформации. Через 12 месяцев после хирургической коррекции ПТО сохранялся стойкий клинический эффект. Признаков пролапса при пробе Вальсальвы не выявлено. Жалоб нет. Данных за воспалительные или объемные изменения в зоне введения МФАТ не получено.
Таким образом, представленное клиническое наблюдение демонстрирует техническую реализуемость и клиническую безопасность комбинированной реконструкции тазового дна собственными тканями с подфасциальным введением микрофрагментированной адипозной ткани.
Проведённое клиническое наблюдение также подтверждает возможность достижения устойчивого анатомического и функционального результата при рецидивной форме ПТО при использовании комбинации нативной пластики и клеточных технологий, которая обеспечивает адекватное восстановление морфофункциональной целостности фасциальных структур тазового дна.
Заключение
Представленный клинический случай демонстрирует возможность эффективного применения комбинированного органосохраняющего подхода при рецидивной форме пролапса тазовых органов III стадии по классификации POP-Q у пациентки репродуктивного возраста с клинически значимыми признаками дисплазии соединительной ткани. Использование нативной пластики в сочетании с подфасциальным введением микрофрагментированной адипозной ткани позволило достичь стойкой анатомической коррекции переднего компартмента, устранения клинических проявлений ПТО и восстановления качества жизни без развития интра- и послеоперационных осложнений в течение 12 месяцев наблюдения.
Применённая методика обеспечила не только механическое восстановление поддержки органов малого таза, но и создала условия для активации репаративных процессов в зоне реконструкции с формированием морфологически и функционально состоятельной соединительной ткани фасции Гальбана. Отсутствие признаков воспалительных изменений, патологического рубцевания и рецидива цистоцеле в динамике наблюдения свидетельствует о клинической безопасности и потенциальной регенеративной эффективности комбинированного подхода.
Особую значимость данный метод приобретает у женщин репродуктивного возраста, для которых принципиально важны сохранение анатомической целостности и минимизация риска имплантат-ассоциированных осложнений. Хирургическое лечение в объёме нативной пластики в сочетании с введением аутологичной МФАТ позволяет целенаправленно воздействовать на качественные характеристики и биомеханические свойства соединительнотканных структур таза, что определяет его перспективность в рамках персонализированной реконструктивной хирургии у пациенток с высоким риском рецидива ПТО .Несмотря на обнадеживающие клинические результаты, представленные данные основаны на единичном наблюдении, что определяет необходимость дальнейших проспективных исследований с расширенной выборкой и длительным периодом наблюдения для объективной оценки эффективности, безопасности и влияния метода на отдалённые функциональные исходы.
Таким образом, сочетание нативной пластики и клеточных технологий представляет собой перспективный вектор развития современной оперативной гинекологии, ориентированный на интеграцию принципов регенеративной медицины в практику хирургического лечения пролапса тазовых органов.
ДЕКЛАРАЦИЯ О НАЛИЧИИ ДАННЫХ: данные, подтверждающие выводы настоящего исследования, можно получить у контактного автора по обоснованному запросу. Данные и статистические методы, представленные в статье, прошли статистическое рецензирование.
DATA AVAILABILITY STATEMENT: Data supporting the findings of this study are available from the corresponding author upon reasonable request. The data and statistical methods presented in the study have been statistically reviewed by the journal editor, a certified biostatistician.
СООТВЕТСТВИЕ ПРИНЦИПАМ ЭТИКИ: проведенное исследование соответствует стандартам Хельсинкской декларации (Declaration Helsinki), одобрено Комитетом по этике Федерального государственного бюджетного учреждения «Уральский научно-исследовательский институт охраны материнства и младенчества» Министерства Здравоохранения Российской Федерации (ул. Репина, д. 1, г. Екатеринбург, 620028, Россия), протокол № 8 от 17.10.2024 г.
ВКЛАД АВТОРОВ:
А.А. Михельсон, М.В. Лазукина — разработка концепции и дизайна исследования; М.В. Лазукина — сбор данных, анализ и интерпретация результатов, обзор литературы, составление черновика рукописи; А.А. Михельсон — критический пересмотр черновика рукописи и формирование его окончательного варианта. Все авторы одобрили финальную версию статьи перед публикацией, выразили согласие нести ответственность за все аспекты работы, подразумевающее надлежащее изучение и решение вопросов, связанных с точностью и добросовестностью любой части работы.
COMPLIANCE WITH ETHICAL STANDARDS: The study complies with the standards of the Declaration of Helsinki, approved by the local ethics committee of the Federal State Budgetary Educational Institution of Higher Education “South Ural State Medical University” of the Ministry of Healthcare of the Russian Federation (64 Vorovskogo Street, Chelyabinsk, 454141, Russia), protocol No. 8 dated 20.09.2021; protocol No. 6 dated 20.10.2025.
AUTHORS’ CONTRIBUTIONS:
Anna A. Mikhelson, Maria V. Lazukina — contributed to the study concept and design. Maria V. Lazukina — collected the data, performed analysis and interpretation of results, conducted the literature review, and drafted the manuscript. Anna A. Mikhelson — critically revised the manuscript and finalized its content. All authors approved the final version of the manuscript prior to publication and agree to be accountable for all aspects of the work, ensuring the integrity and accuracy of any part of the study.
Список литературы
1. Радзинский В.Е., Оразов М.Р., Миннуллина Ф.Ф., Долгов Е.Д. Рецидивирующий пролапс органов малого таза: от эпидемиологии и факторов риска до современных возможностей ранней верификации. Клинический разбор в общей медицине. 2024; 5 (3): 63–67. https://doi.org/10.47407/kr2023.5.3.00375
2. Rickey LM, Markowitz MA. Evaluation and Management of Recurrent Pelvic Organ Prolapse. Curr Urol Rep. 2025;26(1):65. https://doi.org/10.1007/s11934-025-01291-3
3. Jelovsek JE, Gantz MG, Lukacz ES, Zyczynski HM, Sridhar A, Kery C, Chew R, Harvie HS, Dunivan G, Schaffer J, Sung V, Varner RE, Mazloomdoost D, Barber MD. Eunice Kennedy Shriver National Institute of Child Health and Human Development Pelvic Floor Disorders Network. Subgroups of failure after surgery for pelvic organ prolapse and associations with quality of life outcomes: a longitudinal cluster analysis. Am J Obstet Gynecol. 2021;225(5):504.e1–504.e22. https://doi.org/10.1016/j.ajog.2021.06.068
4. Паузина О.А., Аполихина И.А., Романов С.В. и др. Возможные факторы риска развития постоперационного пролапса тазовых органов. Эффективная фармакотерапия. 2023; 19 (7): 28–32. https://doi.org/10.33978/2307-3586-2023-19-7-28-32
5. Оразов М.Р., Радзинский В.Е., Миннуллина Ф.Ф. Клинико-анамнестические факторы риска рецидивирующего пролапса тазовых органов. Практическая медицина. 2024; 22 (6): 18–22. https://pmarchive.ru/kliniko-anamnesticheskie-faktory-riska-recidiviruyushhego-prolapsa-tazovyx-organov/ дата обращения 30.01.2026
6. Мирович Е.Д. Факторы, способствующие возникновению рецидивов пролапса тазовых органов после реконструктивных операций с использованием собственных соединительнотканных структур. Главный врач Юга России. 2024; 4(96): 26–31. http://akvarel2002.ru/assets/files/journal/GlaVrach-%E2%84%964%20(96)%202024%20(4).pdf дата обращения 30.01.2026
7. Schulten SFM, Claas-Quax MJ, Weemhoff M et al. Risk factors for primary pelvic organ prolapse and prolapse recurrence: an updated systematic review and meta-analysis. Am J Obstet Gynecol. 2022;227(2):192–208. https://doi.org/10.1016/j.ajog.2022.04.006
8. Friedman T, Eslick GD, Dietz HP. Risk factors for prolapse recurrence: systematic review and meta-analysis. Int Urogynecol J. 2018;29(1):13–21. https://doi.org/10.1007/s00192-017-3471-7
9. Cattani L, Decoene J, Page AS et al. Pregnancy, labour and delivery as risk factors for pelvic organ prolapse: a systematic review. Int Urogynecol J. 2021;32(7):1623– 1631. https://doi.org/10.1007/s00192-020-04506-y
10. Михельсон А.А., Лазукина М.В., Вараксин А.Н. и др. Эрозия слизистой оболочки влагалища у женщин с хирургической коррекцией пролапса гениталий в постменопаузе. Лечение и профилактика. 2020; 10 (4): 55–64.
11. Hess GF, Nocera F, Taha-Mehlitz S, Christen S, von Strauss Und Torney M, Steinemann DC. Mesh-associated complications in minimally invasive ventral mesh rectopexy: a systematic review. Surg Endosc. 2024;38(12):7073– 7082. https://doi.org/10.1007/s00464-024-11369-7
12. Altman D, Väyrynen T, Engh ME, Axelsen S, Falconer C; Nordic Transvaginal Mesh Group. Anterior colporrhaphy versus transvaginal mesh for pelvic-organ prolapse. N Engl J Med. 2011;364(19):1826–1836. https://doi.org/10.1056/NEJMoa1009521
13. Maher C, Feiner B, Baessler K, Schmid C. Surgical management of pelvic organ prolapse in women. Cochrane Database Syst Rev. 2013;4:CD004014. https://doi.org/10.1002/14651858.CD004014.pub5
14. Huang Y, Wu Q, Tam PKH. Immunomodulatory Mechanisms of Mesenchymal Stem Cells and Their Potential Clinical Applications. Int J Mol Sci. 2022;23(17):10023. https://doi.org/10.3390/ijms231710023
15. McGee C, Baria MR, Gatewood C, Tiwari M, Vasileff WK, Lavender C. Lipoaspiration and Processing to Create Microfragmented Adipose Tissue. Video J Sports Med.2022;2(3). https://doi.org/10.1177/26350254221076855
16. Mantovani M, Gennai A, Russo PR. A new approach to regenerative medicine in gynecology. Int J Gynaecol Obstet. 2022;157(3):536–543. https://doi.org/10.1002/ijgo.13906
17. Fu Q, Song XF, Liao GL, Deng CL, Cui L. Myoblasts differentiated from adipose-derived stem cells to treat stress urinary incontinence. Urology. 2010;75(3):718–723. https://doi.org/10.1016/j.urology.2009.10.003
18. Измайлов А.А., Курбангулов И.Р., Данилко К.В., Слесаренко Я.С., Максимова С.Ю., Фарганов А.Р., Виланд В.Ф., Прантль Л., Фельтхаус О. Первичные результаты применения стромально-васкулярной фракции аутологичной жировой ткани при стрессовом недержании мочи у мужчин. Креативная хирургия и онкология. 2018;8(3):171–175. https://doi.org/10.24060/2076-3093-2018-8-3-171-175
19. Макаров А.В., Тетерина Т.А., Саидова А.С., Арутюнян И.В., Фатхудинов Т.Х., Аполихина И.А., Сухих Г.Т. Клеточные технологии в лечении стрессового недержания мочи у женщин. Урология. 2015;4:108–113. https://doi.org/10.18565/urology.2015.4.108-113
20. Майбородин И.В., Хоменюк С.В., Михеева Т.В., Ярин Г.Ю., Майбородина В.И., Вильгельми И.А., Шевела А.И. Ускорение биодеградации полимера на основе коллагена после адсорбции мезенхимальных мультипотентных стромальных клеток в эксперименте. Трансляционная медицина. 2019;6(5):55-67. https://doi.org/10.18705/2311-4495-2019-6-5-55-67
21. Maene A, Deniz G, Bouland C, Lagneaux L, Philippart P, Buxant F. Suburethral implantation of autologous regenerative cells for female stress urinary incontinence management: Results of a pilot study. Eur J Obstet Gynecol Reprod Biol. 2022;278:38–44. https://doi.org/10.1016/j.ejogrb.2022.08.028
22. Vasudeva P, Tyagi V, Kumar N, Yadav S, Prasad V, Iyer SG. «Mesh free» autologous transobturator mid urethral sling placement for predominant stress urinary incontinence: A pilot study. Neurourol Urodyn. 2021;40(2):659– 665. https://doi.org/10.1002/nau.24599
Об авторах
М. В. ЛазукинаРоссия
Лазукина Мария Валерьевна — к.м.н., старший нaучный сoтрудник, акушер-гинеколог ФГБУ «Урaльский НИИ OMM» Минздрaва России.
ул. Репина, д. 1, Екатеринбург, 620028
Телефон: +7-904-388-83-24
А. А. Михельсон
Россия
Михельсон Анна Алексеевна — доктор медицинских наук, доцент, руководитель отдела сохранения репродуктивной функции, завeдующaя гинeкoлoгичeским oтдeлeниeм ФГБУ «Урaльский НИИ OMM» Минздрaвa России.
ул. Репина, д. 1, Екатеринбург, 620028
Телефон: +7-982-608-28-60
Рецензия
Для цитирования:
Лазукина М.В., Михельсон А.А. Клинический случай хирургического лечения рецидивной формы пролапса тазовых органов у женщины репродуктивного возраста комбинированным методом с применением клеточных технологий. Вестник охраны материнства и младенчества. 2026;3(1):99-107. https://doi.org/10.69964/BMCC-2026-3-1-99-107
For citation:
Lazukina M.V., Mikhelson A.A. Clinical case of surgical management of recurrent pelvic organ prolapse in a woman of reproductive age using a combined approach with cell-based technologies. Bulletin of maternal and child care. 2026;3(1):99-107. (In Russ.) https://doi.org/10.69964/BMCC-2026-3-1-99-107
JATS XML









