Перейти к:
Аутологичный фибриновый клей, обогащенный тромбоцитами, в хирургии эндометриоидных кист яичников: стратегия сохранения овариального резерва
https://doi.org/10.69964/BMCC-2026-3-1-89-98
Аннотация
Введение. Эндометриомы являются одним из наиболее частым гинекологических заболеваний. Хирургическое удаление эндометриомы рассматривается как стандарт тактики ведения при эндометриомах крупных размеров и/или сопровождающихся болевым синдромом. Однако, несмотря на клиническую эффективность удаления очага, данный подход сопряжён с рядом репродуктивных рисков.
Цель исследования: сравнить влияние двух методов интраоперационного гемостаза (аутологичного фибринового клея, обогащенного тромбоцитами, и стандартной биполярной коагуляции) на сохранение овариальной функции у пациенток после лапароскопической цистэктомии эндометриоидных кист яичников.
Материалы и методы: Проведено проспективное когортное сравнительное исследование, включившее 72 пациентки репродуктивного возраста с эндометриомами яичников. Пациентки распределены в две группы по 36 человек. Группы были сопоставимы по исходным клинико-анамнестическим, гормональным и ультразвуковым характеристикам. Всем выполнена лапароскопическая цистэктомия. В группе 1 гемостаз осуществляли аутологичным фибриновым клеем, обогащенным тромбоцитами, в группе 2 – биполярной коагуляцией. До операции и через 6 месяцев оценивали: уровни АМГ, ФСГ, СА-125; объем яичников, КАФ, индекс резистентности яичниковой артерии (IR) по данным УЗИ.
Результаты: Через 6 месяцев после операции в группе фибринового клея уровень АМГ был статистически значимо выше, чем в группе коагуляции: 3,85 (1,89–7,17) против 2,1 (1,1–4,3) нг/мл, р=0,03. Уровень ФСГ в группе 2 повысился (р=0,03), в группе 1 – не изменился. КАФ в оперированном яичнике в основной группе увеличился (р=0,03), в группе сравнения – не изменился. IR значимо снизился в обеих группах (р < 0,01). Уровень СА-125 после операции был ниже в группе 1 (р=0,02).
Заключение: Использование аутологичного фибринового клея, обогащенного тромбоцитами, для гемостаза при лапароскопической цистэктомии эндометриом позволяет значимо лучше сохранить овариальную функцию по сравнению с биполярной коагуляцией. Метод может быть рекомендован как приоритетный у пациенток, заинтересованных в сохранении фертильности.
Ключевые слова
Для цитирования:
Михельсон А.А., Кудрявцева Е.В., Тимерханова Е.О., Мелкозерова О.A., Семенов Ю.А., Лазукина М.В. Аутологичный фибриновый клей, обогащенный тромбоцитами, в хирургии эндометриоидных кист яичников: стратегия сохранения овариального резерва. Вестник охраны материнства и младенчества. 2026;3(1):89-98. https://doi.org/10.69964/BMCC-2026-3-1-89-98
For citation:
Mikhelson A.A., Kudryavtseva E.V., Timerkhanova E.O., Melkozerova O.A., Semenov Yu.A., Lazukina M.V. Autologous platelet-rich fibrin glue in surgery of endometrioid ovarian cysts: a strategy for preserving ovarian reserve. Bulletin of maternal and child care. 2026;3(1):89-98. (In Russ.) https://doi.org/10.69964/BMCC-2026-3-1-89-98
Введение
Эндометриоз яичников характеризуется наличием в яичниках ткани, подобной эндометрию, которая разрастается и образует кистозное образование (эндометриому). Эндометриомы являются одним из наиболее частым гинекологических заболеваний и встречаются у 17–44% женщин среди больных эндометриозом [1–3]. В настоящее время хирургическое удаление эндометриомы, в частности лапароскопическая цистэктомия, рассматривается как стандарт тактики ведения при эндометриомах крупных размеров (более 3 см в диаметре) и/или сопровождающихся болевым синдромом [1][4]. Однако, несмотря на клиническую эффективность удаления очага, данный подход сопряжён с рядом репродуктивных рисков.
Известно, что пациентки с эндометриомами нередко страдают нарушением фертильности [2][5][6]. Патогенетические механизмы эндометриоз-ассоциированного бесплодия многофакторны и включают снижение качества ооцитов вследствие хронического воспаления, изменения фолликулярной микросреды, а также уменьшение овариального резерва, обусловленное повышенным окислительным стрессом и локальной воспалительной реакцией в ткани яичника [7–9]. Дополнительным фактором риска снижения овариального резерва является само хирургическое вмешательство. При выполнении цистэктомии возможно непреднамеренное удаление неизменённой кортикальной ткани яичника, содержащей примордиальные фолликулы, что потенциально ведёт к уменьшению функционального фолликулярного пула [1]. В этой связи особое значение приобретает не только объём хирургического удаления, но и метод достижения интраоперационного гемостаза, который также способен оказывать повреждающее воздействие на овариальную ткань [10].
На сегодняшний день наиболее широко применяемым методом гемостаза при лапароскопической цистэктомии является биполярная электрокоагуляция. Вместе с тем термическое воздействие может усугублять ишемическое и коагуляционное повреждение коркового слоя яичника, что стимулирует поиск альтернативных, органосохраняющих технологий [10].
Несмотря на значительное количество исследований, оптимальный хирургический подход к лечению эндометриом, обеспечивающий баланс между радикальностью удаления и сохранением овариальной функции, до настоящего времени остаётся предметом дискуссий. Сложность и неоднородность имеющихся данных обосновывают необходимость индивидуализации лечебной тактики с выбором наименее травматичных методов хирургии и гемостаза [11].
Цель исследования: сравнить влияние двух методов интраоперационного гемостаза (аутологичного фибринового клея, обогащенного тромбоцитами, и стандартной биполярной коагуляции) на сохранение овариальной функции у пациенток после лапароскопической цистэктомии эндометриоидных кист яичников.
Материалы и методы
Было проведено проспективное когортное сравнительное исследование.
В исследование включено 72 женщины репродуктивного возраста с эндометриомами яичников, имеющие показания для оперативного лечения.
Всеми пациентками было подписано информированное добровольное согласие на оперативное лечение и на участие в исследовании.
Всем пациенткам лапароскопическим доступом была проведена цистэктомия. Хирургическое лечение проводилось лапароскопическим доступом с использованием стойки с 3D HD объемной визуализацией (Einstein Vision). Выполнялась энуклеация стенки кисты в пределах неизмененной ткани яичника. В группу 1 (основная) были включены пациентки, которым с целью достижения гемостаза во время проведения лапароскопической цистэктомии применялся аутологичный фибриновый клей, обогащенный тромбоцитами. В группу 2 (группа сравнения) — пациентки, которым во время лапароскопической цистэктомии проводилась биполярная коагуляция ложа кисты. В каждую группу было включено по 36 участниц. Диагноз «эндометриома» во всех случаях был подтвержден с помощью гистологического исследования.
Для распределения пациенток по группам была применена рандомизация методом блоков с использованием компьютерного генератора случайных чисел. Размер блока составлял 4 участницы, что обеспечило равномерное распределение в течение всего периода набора.
Для оценки овариального резерва (ОР) у всех участниц исследования до операции и через 6 месяцев после нее проводили оценку гормонального профиля: определяли уровни антимюллерова гормона (АМГ) и фолликулостимулирующего гормона (ФСГ) на 2–5‑й день менструального цикла. В раннюю фолликулярную фазу (5–7‑й день менструального цикла) путем трансвагинального ультразвукового исследования (УЗИ) определяли объем яичников, количество антральных фолликулов (КАФ), показатели кровотока в яичниках (индекс резистентности яичниковой артерии в пораженном яичнике — IRЯА). До оперативного лечения оценивались ультразвуковые характеристики образования яичников.
Для дополнительного контроля исходной сопоставимости исследуемых групп и эффективности хирургического лечения эндометриоза мы исследовали до и через 6 месяцев после оперативного лечения показатель СА-125.
Статистическая обработка данных выполнялась с помощью программного обеспечения Jamovi (версия 2.3) [12].
Для проверки нормальности распределения использовался критерий Колмогорова-Смирнова. Распределение не соответствовало нормальному, поэтому были применены непараметрические методы статистической обработки. Для количественных показателей указывалась медиана (Ме) с интерквартильным размахом между 1‑м и 3‑м квартилями (К1–К3). Для оценки значимости различий между исследуемыми группами был применен критерий Манна-Уитни. Для оценки значимости различий для связанных выборок (значение показателей внутри одной группы до и после операции) применялся тест Вилкоксона. Различия считались статистически значимыми при р<0,05
Результаты
Средний возраст пациенток в исследуемых группах составил в группе 1 — 34 (27,8-37) лет, в группе 2 — 33 (27-35) лет (р=0,189). Средний ИМТ был соответственно 21,1 (18,7-25,1) кг/м² и 22,3 (18,6-24,3) кг/м² (р=0,563). По частоте встречаемости соматической и гинекологической патологии в анамнезе и характеру менструального цикла статистически значимых различий между исследуемыми группами также выявлено не было.
Далее мы сравнили исходные УЗИ-характеристики. Результаты представлены в таблице 1. Статистически значимых различий между исследуемыми группами не выявлено.
Таблица 1. Показатели УЗИ в исследуемых группах до оперативного лечения.
Table 1. Ultrasound indicators in the study groups before surgery.
Показатель | Группа 1 | Группа 2 | р |
Длина эндометриомы, мм | 40 (35-48,5) | 39 (35,8-45) | 0,66 |
Толщина эндометриомы, мм | 30 (25-35) | 29,5 (25,8-35,5) | 0,55 |
Ширина эндометриомы, мм | 36,5 (32,8-43,7) | 35 (30,8-39) | 0,28 |
Объем эндометриомы, см³ | 23,1 (15,2-34) | 22,5 (15,7-32,7) | 0,39 |
Объем пораженного яичника, см³ | 36 (24,9-57,4) | 35,4 (22-50,8) | 0,13 |
КАФ в пораженном яичнике, N | 5 (4-6) | 5 (4-7) | 0,72 |
КАФ, всего, N | 12 (10-16) | 13 (10-16) | 0,67 |
IRЯА | 0,76 (0,74-0,81) | 0,77 (0,75-0,82) | 0,52 |
Объем остаточной здоровой ткани пораженного яичника, см3 | 10,6 (7,76-19,2) | 9,9 (5,34-21,1) | 0,37 |
По уровню АМГ, ФСГ и СА-125 существенных различий между исследуемыми группами до операции также не было – см. таблицу 2.
Таблица 2. Уровень АМГ, ФСГ, СА-125 в исследуемых группах до операции.
Table 2. Levels of AMH, FSH, CA-125 in the study groups before surgery.
Показатель | Группа 1 | Группа 2 | р |
АМГ, нг/мл | 3,24 (1,1-6,22) | 3,4 (1,31-6,47) | 0,41 |
ФСГ, мМЕ/л | 6,21 (5,28-8,09) | 5,83 (5,5-7,65) | 0,75 |
СА-125, ЕД/мл | 46,2 (36,6-66,7) | 43,1 (39,6-63,7) | 0,56 |
Все показатели были оценены повторно через 6 месяцев после операции. Результаты представлены в таблице 3.
Таблица 3. Исследуемые показатели через 6 месяцев после оперативного лечения
Table 3. Studied parameters 6 months after surgical treatment
Показатель | Группа 1 | Группа 2 | р |
АМГ, нг/мл | 3,85 (1,89-7,17) | 2,1 (1,1-4,3) | 0,03 |
ФСГ, мМЕ/л | 6,8 (5,9-7,88) | 7,9 (6,4-8,9) | 0,09 |
СА-125, ЕД/мл | 28,9 (22,2-31,1) | 31,9 (28,1-36,7) | 0,02 |
КАФ в оперированном яичнике, N | 8 (7-10) | 6 (5-9) | 0,33 |
КАФ, всего, N | 14 (11-17) | 13 (11-15) | 0,55 |
IRЯА | 0,56 (0,53-0,59) | 0,55 (0,52-0,61) | 0,89 |
Получены статистически значимые различия по уровню АМГ – он оказался выше в основной группе, где во время лапароскопической цистэктомии применялся аутологичный фибриновый клей, обогащенный тромбоцитами. Уровень ФСГ в группе 1 при этом был несколько выше, хотя различия не достигли статистической значимости. В группе сравнения, где с целью достижения гемостаза проводилась биполярная коагуляция ложа кисты, через 6 месяцев после операции существенно выше было значение показателя СА-125.
При сравнении показателей внутри исследуемых групп до операции и через 6 месяцев после операции также выявлен ряд закономерностей.
IR существенно снизился в обеих группах (p<0,01). СА-125 после операции также стал через 6 месяцев после операции в обеих группах ниже (p<0,01).
В группе 1 уровень АМГ через 6 месяцев после операции в среднем был выше, однако различия статистически не значимы (р=0,75). Уровень ФСГ также существенно не изменился (р=0,23). Суммарное КАФ до и после операции было сопоставимым, однако КАФ в оперированном яичнике стало больше (р=0,03). При анализе аналогичных параметров в группе сравнения результаты были несколько иными. В группе 2 уровень АМГ через 6 месяцев после операции снизился (р=0,02), а ФСГ стал выше (р=0,03). КАФ существенно не изменилось. Динамике уровней АМГ и ФСГ отражена на рисунке.
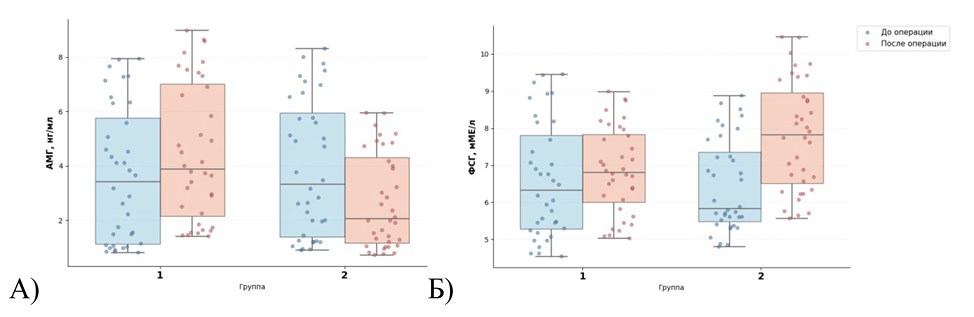
Рисунок. Уровень АМГ (А) и ФСГ (Б) до оперативного лечение и через 6 месяцев после него
Figure. AMH (A) and FSH (B) levels before and 6 months after surgery
Обсуждение результатов
Преимущества использования фибриновых герметиков в хирургии исследуются с 80‑х гг. ХХ века [13][14]. Использование подобных средств гемостаза патогенетически обосновано. Известно, что предотвращение местного кровотечения, происходящего в ответ на ранение, достигается за счет агрегации тромбоцитов и запуска каскада гемостаза. Образовавшийся сгусток крови останавливает кровотечение и затем функционирует как временная матрица для заживления раны. Здесь ключевую роль играют фибриноген и фибриновые волокна — они служат каркасами для регенерации тканей и способствуют миграции клеток. Фибрин также является важным модулятором заживления [15][16].
Результаты проведенного исследования демонстрируют значимое преимущество использования аутологичного фибринового клея, обогащенного тромбоцитами, для гемостаза при лапароскопической цистэктомии эндометриом яичников с точки зрения сохранения овариальной функции.
Ключевым результатом является статистически значимое более высокое значение уровня АМГ через 6 месяцев наблюдения в группе, где применялся фибриновый клей, по сравнению с группой биполярной коагуляции. Этот вывод подтверждается динамикой внутри групп: в группе сравнения зафиксировано достоверное снижение уровня АМГ и повышение уровня ФСГ после операции. В основной группе аналогичной негативной динамики маркеров овариального резерва выявлено не было, что свидетельствует о щадящем воздействии предлагаемого метода гемостаза на овариальную паренхиму.
Примечательным является факт увеличения количества антральных фолликулов (КАФ) в оперированном яичнике в основной группе при стабильном суммарном КАФ. Этот парадоксальный на первый взгляд результат может быть объяснен несколькими механизмами. Во-первых, отсутствие термической травмы и последующего фиброза могло улучшить перфузию коркового слоя, что подтверждается значимым снижением индекса резистентности (IR) в обеих группах. Во-вторых, биологически активные факторы роста, содержащиеся в обогащенном тромбоцитами фибриновом клее, потенциально могут оказывать стимулирующее влияние на васкуляризацию и тканевую регенерацию. Таким образом, предложенный метод не только минимизирует ятрогенное повреждение, но и может создавать условия для частичного восстановления овариальной ткани после удаления кисты.
Наши результаты соответствуют данным научной литературы. В частности, в систематическом обзоре, проведенном Lin Y. et al. (2024) было продемонстрировано, что по сравнению с группой, получавшей биполярную электрокоагуляцию, у пациенток с эндометриомами в группе, получавшей нетермическую гемостатическую терапию, наблюдались значительно более высокие послеоперационные уровни АМГ через 1, 3, 6 и 12 месяцев. КАФ у пациенток с эндометриомами в группе, получавшей электрокоагуляцию, при этом после операции снижалось [10]. Авторы пришли к заключению, что при лапароскопической цистэктомии по поводу эндометриом яичников нетермические методы гемостаза связаны с более эффективным сохранением ОР по сравнению с биполярной электрокоагуляцией [10]. Аналогичные выводы были сделаны также Chung J.P.W. et al. (2021) — в группе с гемостатическим герметиком в течение года после операции по поводу овариальной эндометриомы наблюдалось большее КАФ, по сравнению с группой, где проводилась электрокоагуляция [17].
В настоящее время результатов исследований, демонстрирующих преимущества фибринового клея именно в хирургии эндометриоза, в международной научной литературе не представлено. Однако есть данные, что данный метод гемостаза может применяться для уменьшения травматизации тканей и улучшении репродуктивных результатов при бесплодии, ассоциированным с трубным фактором [13]. Предполагается, что использование фибринового клея способствует профилактике образования послеоперационных спаек [14]. Однако в нашем исследование выраженность спаечного процесса после проведенного оперативного лечения мы не исследовали.
Снижение уровня сывороточного СА-125 в обеих группах подтверждает радикальность и эффективность проведенного хирургического лечения в равной степени. Однако тот факт, что через 6 месяцев его значение в группе коагуляции оставалось статистически значимо выше, чем в основной группе, требует отдельного осмысления. Мы предполагаем, что сохраняющаяся более высокая воспалительная или ишемическая активность в ткани яичника после термического воздействия может поддерживать несколько повышенный уровень этого неспецифического маркера.
Важно подчеркнуть, что исходные характеристики, включая параметры ОР и размеры эндометриом, в группах были сопоставимы. Это исключает систематическую ошибку и позволяет с высокой достоверностью связать выявленные различия именно с методом гемостаза.
Ограничения исследования включают относительно небольшой срок наблюдения (6 месяцев) и отсутствие оценки отдаленных репродуктивных исходов (наступления спонтанной беременности, необходимости и результатов применения вспомогательных репродуктивных технологий).
Заключение
Полученные данные свидетельствуют, что выбор метода интраоперационного гемостаза оказывает влияние на послеоперационную овариальную функцию. Применение аутологичного фибринового клея, обогащенного тромбоцитами, демонстрирует значимые преимущества перед традиционной биполярной коагуляцией.
Ключевым патофизиологическим механизмом, лежащим в основе этого преимущества, является минимизация ятрогенного термического повреждения стромы яичника и его сосудистой сети. Таким образом, предложенная методика представляет собой клинически значимую оптимизацию хирургического этапа лечения эндометриом, напрямую соответствующую принципам фертильность-сберегающей хирургии. Она позволяет нейтрализовать одно из основных негативных последствий цистэктомии –снижение овариального резерва.
ДЕКЛАРАЦИЯ О НАЛИЧИИ ДАННЫХ: данные, подтверждающие выводы настоящего исследования, можно получить у контактного автора по обоснованному запросу. Данные и статистические методы, представленные в статье, прошли статистическое рецензирование.
СООТВЕТСТВИЕ ПРИНЦИПАМ ЭТИКИ: проведенное исследование соответствует стандартам Хельсинкской декларации (Declaration Helsinki), одобрено Комитетом по этике Федерального государственного бюджетного учреждения «Уральский научно-исследовательский институт охраны материнства и младенчества» Министерства Здравоохранения Российской Федерации (ул.Репина, д. 1, г. Екатеринбург, 620028, Россия), протокол № 5 от 04.04.2025 г.
DATA AVAILABILITY STATEMENT: data supporting the findings of this study are available from the corresponding author upon reasonable request. The data and statistical methods presented in the article have undergone statistical review.
COMPLIANCE WITH ETHICAL STANDARDS: the research conducted complies with the standards of the Declaration of Helsinki, approved by the Ethics Committee of the Federal State Budgetary Institution “Ural Research Institute for Maternal and Infant Protection” of the Ministry of Health of the Russian Federation (Repin Str., 1, Ekaterinburg, 620028, Russia). Protocol No. 5 of 04.04.2025.
ВКЛАД АВТОРОВ:
А.А. Михельсон — разработка концепции и дизайна исследования, анализ и интерпретация результатов; Е.В. Кудрявцева – статистическая обработка, анализ и интерпретация результатов, составление черновика рукописи; Е.О. Тимерханова, М.В. Лазукина — сбор данных, анализ и интерпретация результатов, составление черновика рукописи; О.А. Мелкозерова, Ю.А. Семенов — критический пересмотр, редактирование рукописи и формирование его окончательного варианта. Все авторы одобрили финальную версию статьи перед публикацией, выразили согласие нести ответственность за все аспекты работы, подразумевающее надлежащее изучение и решение вопросов, связанных с точностью и добросовестностью любой части работы.
AUTHOR CONTRIBUTIONS:
Anna A. Mikhelson — development of the study concept and design, analysis and interpretation of results; Eleva V. Kudryavtseva — statistical processing, analysis and interpretation of results, drafting the manuscript; Ekaterina O. Timerkhanova, Maria V. Lazukina — data collection, analysis and interpretation of results, drafting the manuscript; Oxana A. Melkozerova, Yuri A. Semenov — critical revision, editing of the manuscript and formation of its final version. All authors approved the final version of the article before publication and agreed to be responsible for all aspects of the work, implying proper investigation and resolution of issues related to the accuracy or integrity of any part of the work.
Список литературы
1. Kalra R., McDonnell R., Stewart F., Hart R.J., Hickey M., Farquhar C. Excisional surgery versus ablative surgery for ovarian endometrioma. Cochrane Database Syst Rev. 2024; 11: CD004992. https://doi.org/10.1002/14651858.CD004992.pub4
2. Михельсон А.А., Телякова М.И., Окулова Е.А., Мелкозерова О.А. Выбор хирургических методов лечения эндометриоидных кист яичников с целью сохранения овариального резерва (обзор литературы). Проблемы Репродукции. 2020;26:57–64.
3. Сухих Г.Т., Серов В.Н., Адамян Л.В., Баранов И.И., Беженарь В.Ф., Габидуллина Р.И., et al. Алгоритмы ведения пациенток с эндометриозом: согласованная позиция экспертов Российского общества акушеров-гинекологов. Акушерство и Гинекология. 2023;5:159–176. https://doi.org/10.18565/aig.2023.132.
4. Дубровина С.О., Берлим Ю.Д., Александрина А.Д., Вовкочина М.А., Богунова Д.Ю., Гимбут В.С., и др. Современные представления о диагностике и лечении эндометриоза. Акушерство и Гинекология. 2023;146–153. https://doi.org/10.18565/aig.2023.43
5. Goyri E., Kohls G., Garcia-Velasco J.. IVF stimulation protocols and outcomes in women with endometriosis. Best Pract Res Clin Obstet Gynaecol 2024; 92: 102429. https://doi.org/10.1016/j.bpobgyn.2023.102429
6. Окулова Е.О., Мелкозерова О.А., Михельсон А.А., Третьякова Т.Б., Чистякова Г.Н., Лимановская О.В., и др. Прогнозирование риска снижения овариального резерва после хирургического лечения пациенток с глубоким инфильтративным эндометриозом с использованием искусственного интеллекта. Российский Вестник Акушера-Гинеколога. 2022;24:92–109.
7. Адамян Л.В., Андреева Е.Н. Эндометриоз и его глобальное влияние на организм женщины. Проблемы Репродукции. 2022;28:54–64. https://doi.org/10.17116/repro20222801154
8. Кудрявцева Е.В., Мангилева Я.А., Полушина Л.Г., Максимова А.Ю., Копенкин М.А., Зорников Д.Л., и др. Исследование уровней биомаркеров воспаления и ангиогенеза в различных биологических жидкостях у женщин с наружным генитальным эндометриозом. Акушерство и Гинекология. 2025;:112–120. https://doi.org/10.18565/aig.2025.116
9. Мангилева Я.А., Чижова А.В., Кудрявцева Е.В., Исламиди Д.К., Геец А.В. Значение состава перитонеальной жидкости в генезе бесплодия у женщин с эндометриозом яичников. Вестник Уральской Медицинской Академической Науки. 2022;19(2):82–94. https://doi.org/10.22138/2500-0918-2022-19-2-82-94
10. Lin Y.-H., Hsia L.-H., Huang Y.-Y., Chang H.-J., Lee T.-H. Potential damage to ovarian reserve from laparoscopic electrocoagulation in endometriomas and benign ovarian cysts: a systematic review and meta-analysis. J Assist Reprod Genet 2024; 41: 2727–38. https://doi.org/10.1007/s10815-024-03227-1
11. Daniilidis A., Grigoriadis G., Kalaitzopoulos D.R., Angioni S., Kalkan Ü., Crestani A. et al. Surgical Management of Ovarian Endometrioma: Impact on Ovarian Reserve Parameters and Reproductive Outcomes. J Clin Med 2023; 12: 5324. https://doi.org/10.3390/jcm12165324
12. The jamovi project 2022. www.jamovi.org
13. Papageorgiou D., Pergialiotis V., Sapantzoglou I., Bikouvaraki E.S., Salakos N., Kykalos S. et al. The Effect of Fibrin Sealants on Tubal Reanastomosis: A Comprehensive Review of the Literature. J Pers Med 2025; 16: 12. https://doi.org/10.3390/jpm16010012
14. Takeuchi H., Toyonari Y., Mitsuhashi N., Kuwabara Y. Effects of fibrin glue on postsurgical adhesions after uterine or ovarian surgery in rabbits. J Obstet Gynaecol Res 1997; 23: 479–84. https://doi.org/10.1111/j.1447-0756.1997.tb00876.x.
15. Bayer I/S. Advances in Fibrin-Based Materials in Wound Repair: A Review. Molecules 2022; 27. https://doi.org/10.3390/molecules27144504
16. Brown K.G.M., Solomon M.J. Topical haemostatic agents in surgery. Br J Surg 2024;111. https://doi.org/10.1093/bjs/znad361
17. Chung J.P.W., Law T.S.M., Mak J.S.M., Sahota D.S., Li T.C. Ovarian reserve and recurrence 1 year post-operatively after using haemostatic sealant and bipolar diathermy for haemostasis during laparoscopic ovarian cystectomy. Reprod Biomed Online 2021; 43: 310–8. https://doi.org/10.1016/j.rbmo.2021.05.003
Об авторах
А. А. МихельсонРоссия
Михельсон Анна Алексеевна — доктор медицинских наук, доцент, заведующая отделением сохранения репродуктивной функции ФГБУ «НИИ OMM» МЗ РФ.
ул. Репина, д. 1, Екатеринбург, 620028
Е. В. Кудрявцева
Россия
Кудрявцева Елена Владимировна — доктор медицинских наук, доцент, ведущий научный сотрудник отделения сохранения репродуктивной функции ФГБУ «НИИ OMM» МЗ РФ.
ул. Репина, д. 1, Екатеринбург, 620028
Тел.: +7 (922) 616 40 12
Е. О. Тимерханова
Россия
Тимерханова Екатерина Олеговна — к.м.н., научный сотрудник отделения сохранения репродуктивной функции ФГБУ «НИИ OMM» МЗ РФ.
ул. Репина, д. 1, Екатеринбург, 620028
О. A. Мелкозерова
Россия
Мелкозерова Оксана Александровна — доктор медицинских наук, профессор, проректор по научно-исследовательской и инновационной деятельности ФГБОУ ВО «УГМУ» МЗ РФ; заместитель директора по научной работе ФГБУ «НИИ OMM» МЗ РФ.
ул. Репина, д. 1, Екатеринбург, 620028; ул. Репина, д.3, Екатеринбург, 620028
Ю. А. Семенов
Россия
Семенов Юрий Алексеевич — доктор медицинских наук, доцент, проректор по ректор ФГБОУ ВО «УГМУ» МЗ РФ.
ул. Репина, д. 1, Екатеринбург, 620028
М. В. Лазукина
Россия
Лазукина Мария Валерьевна — к.м.н., старший нaучный сoтрудник, акушер-гинеколог ФГБУ «Урaльский НИИ OMM» Минздрaва России.
ул. Репина, д. 1, Екатеринбург, 620028
Телефон: +7-904-388-83-24
Рецензия
Для цитирования:
Михельсон А.А., Кудрявцева Е.В., Тимерханова Е.О., Мелкозерова О.A., Семенов Ю.А., Лазукина М.В. Аутологичный фибриновый клей, обогащенный тромбоцитами, в хирургии эндометриоидных кист яичников: стратегия сохранения овариального резерва. Вестник охраны материнства и младенчества. 2026;3(1):89-98. https://doi.org/10.69964/BMCC-2026-3-1-89-98
For citation:
Mikhelson A.A., Kudryavtseva E.V., Timerkhanova E.O., Melkozerova O.A., Semenov Yu.A., Lazukina M.V. Autologous platelet-rich fibrin glue in surgery of endometrioid ovarian cysts: a strategy for preserving ovarian reserve. Bulletin of maternal and child care. 2026;3(1):89-98. (In Russ.) https://doi.org/10.69964/BMCC-2026-3-1-89-98
JATS XML









