Перейти к:
Ключевые аспекты течения неонатальной адаптации у недоношенных новорожденных гестационного возраста 32–36 недель 6 дней, кишечник которых колонизирован Klebsiella pneumoniae с генами uge, fim и kfu
https://doi.org/10.69964/BMCC-2026-3-1-78-88
Аннотация
Введение. Современные молекулярно-генетические исследования опровергают прежнюю концепцию о стерильности внутриутробной среды: установлено, что желудочно-кишечный тракт плода уже содержит микроорганизмы, в том числе Klebsiella pneumoniae (КР), чья колонизация определяется комплексом перинатальных факторов (гестационный возраст, характер вскармливания, пребывание в отделении реанимации и интенсивной терапии (ОРИТ), антибиотикотерапия). Исход колонизации кишечника недоношенных — от бессимптомного носительства до развёрнутой инфекции — определяется состоянием местной защиты слизистой, иммунологической реактивностью ребёнка и вирулентными свойствами Klebsiella pneumoniae. Наличие у КР генетически детерминированных факторов вирулентности (генов fim, kfu, uge) и их потенциальное влияние на течение неонатального периода обосновывают актуальность настоящего исследования.
Цель исследования. Изучить ключевые аспекты течения неонатальной адаптации у недоношенных новорожденных гестационного возраста 32–36 недель 6 дней, кишечник которых колонизирован Klebsiella pneumoniae с генами uge, fim и kfu.
Материалы и методы. Проведено обследование 30 новорожденных гестационного возраста 32-36 недель 6 дней, кишечник которых колонизирован Klebsiella pneumoniae (KP). В зависимости от геноварианта штаммов дети были подразделены на три группы: 1-я группа — недоношенные, колонизированные KP геном uge (n=6), 2-я — uge+fim (n=16), 3-я - kfu+uge+fim (n=8). Проведена комплексная оценка клинических, лабораторных, инструментальных и микробиологических показателей у недоношенных детей. Детекция генов uge, fim и kfu проводилась методом полимеразной цепной реакцией (ПЦР) в режиме реального времени.
Результаты исследования. Показано, что антропометрические данные, оценка по шкале Апгар, во всех группах были сопоставимы. У недоношенных с генами kfu+uge+fim установлены наиболее низкие показатели гемоглобина (113,37±14,82 г/л) и гематокрита (33,73±4,56%) на 10–14-е сутки жизни (р<0,001), максимальная продолжительность респираторной поддержки (2,06±1,24 дня; р=0,012) и антибактериальной терапии (19,0±5,60 суток; р=0,005), а также ухудшение состояния с переводом в ОРИТ в 37,5% случаев. У детей с генотипом uge+fim чаще регистрировались перинатальные инфекции (81,25%; р<0,017) и сохранялась колонизация K. pneumoniae при выписке (100%; р=0,002).
Заключение. Поскольку недоношенные дети, колонизированные K. pneumoniae с генотипами uge+fim и kfu+uge+fim, к моменту выписки остаются бактериовыделителями, на фоне иммунной незрелости сохраняется риск реализации клебсиеллёзной инфекции и обосновывает необходимость их диспансерного наблюдения.
Ключевые слова
Для цитирования:
Маханёк А.А., Чистякова Г.Н., Устюжанин А.В., Ремизова И.И. Ключевые аспекты течения неонатальной адаптации у недоношенных новорожденных гестационного возраста 32–36 недель 6 дней, кишечник которых колонизирован Klebsiella pneumoniae с генами uge, fim и kfu. Вестник охраны материнства и младенчества. 2026;3(1):78-88. https://doi.org/10.69964/BMCC-2026-3-1-78-88
For citation:
Mahanek A.A., Chistyakova G.N., Ustyuzhanin A.V., Remizova I.I. Key aspects of neonatal adaptation in preterm newborns of gestational age 32–36 weeks and 6 days, whose intestines are colonized by Klebsiella pneumoniae with uge, fim and kfu genes. Bulletin of maternal and child care. 2026;3(1):78-88. (In Russ.) https://doi.org/10.69964/BMCC-2026-3-1-78-88
Введение
Долгое время доминировала классическая концепция о стерильности внутриутробной среды, согласно которой колонизация кишечника новорождённого начиналась после рождения — при контакте с микробиоценозом матери (через родовые пути) и факторами окружающей среды [1]. Однако эта теория, основанная на ранних культуральных исследованиях, в настоящее время подвергается критическому пересмотру благодаря данным современных молекулярно генетических методов (в частности, секвенированию гена 16S рРНК) [2][3]. Полученные результаты свидетельствуют о том, что меконий и желудочно кишечный тракт плода уже содержат микроорганизмы, которые могут оказывать потенциальное влияние на последующее развитие как инфекционной, так и неинфекционной патологии [4–7].
Одним из клинически значимых представителей условно-патогенных микроорганизмов, являющихся частью нормального микробиоценоза кишечника новорождённых и колонизирующих желудочно-кишечный тракт в условиях комменсализма, является Klebsiella pneumoniae (КР). КР обладает выраженным патогенным потенциалом и способна вызывать оппортунистические инфекции у иммунокомпрометированных лиц, в том числе у недоношенных новорождённых [8–10].
Процесс колонизации кишечника новорождённого Klebsiella pneumoniae — это многофакторный процесс, опосредованный комплексом перинатальных факторов, влияющих как на риск заселения, так и на его клинические исходы [11]. Ключевую роль играет гестационный возраст: у недоношенных детей, особенно рождённых до 32‑й недели беременности, механизмы колонизационной резистентности кишечника существенно снижены, что повышает восприимчивость к адгезии условно-патогенных микроорганизмов [12]. Кроме того, существенное значение имеет сопутствующая патология, связанная с недоношенностью: респираторный дистресс-синдром, ишемически-гипоксические поражения центральной нервной системы (ЦНС), нарушения моторной функции кишечника и расстройства мукозального иммунитета [12][13]. Характер вскармливания — важный модифицируемый фактор. Грудное молоко содержит олигосахариды, стимулирующие рост бифидо- и лактобактерий, а также секреторные иммуноглобулины (SIgA), подавляющие адгезию K. pneumoniae к слизистой оболочки кишечника [14][15][16]. Искусственное вскармливание, напротив, лишено этих защитных компонентов за счёт высокого содержания железа и буферных свойств молочных адаптированных смесей и создаёт благоприятную среду для колонизации КР. Длительное пребывание недоношенных детей в отделении реанимации и интенсивной терапии (ОРИТ), особенно в сочетании с инвазивными манипуляциями (интубация трахеи и проведение ИВЛ, катетеризация сосудов для проведения парентерального питания, зондовое кормление), существенно повышает риск колонизации кишечника K. pneumoniae за счёт контакта с госпитальными штаммами и нарушения естественных защитных барьеров [12][17][18]. Массивная антибиотикотерапия подавляет индигенную микрофлору и формирует условия для роста устойчивых энтеробактий [12][17][19].
Исход колонизации кишечника K. pneumoniae — от бессимптомного носительства до развёрнутой инфекции определяется состоянием локальной защитой слизистой оболочки кишечника, уровнем иммунологической реактивности недоношенного ребенка и вирулентными свойствами самого микроорганизма. Помимо хорошо изученных генов антибиотикорезистентности, у KР выделен широкий спектр генетически детерминированных факторов вирулентности, которые в совокупности определяют ее роль инфекционном потенциале [20]. По результатам современных исследований выделяют следующие факторы вирулентности КР: фимбрии 1 (кодируются геном fim) и 3 (кодируется генным кластером mrk) типов, которые обеспечивают прикрепление и адгезию к слизистой оболочке кишечника, участвуют в формировании биопленок; сидерофоры – образование комплексных соединений железа (Fe3⁺) и его транспорт (ген вирулентности kfu); капсула и липополисахарид – защита микроорганизма от системы комплемента и фагоцитов, высвобождение эндотоксина. Ген uge кодирует фермент уридин-дифосфат-галактуронат-4-эпимеразу (UDP-galacturonate 4-epimerase), который участвует в биосинтезе липополисахарида (ЛПС) — ключевого компонента внешней мембраны грамотрицательных бактерий [21–24].
Генетически обусловленные детерминанты вирулентности K. pneumoniae существенно влияют на вероятность транслокации возбудителя и реализацию инфекционного процесса у новорождённых. В литературе представлены лишь сведения о микробиологической характеристики и роли факторов патогенности в неонатальном периоде, при этом их влияние на клиническую адаптацию недоношенных детей системно не анализировалось, что послужило основанием для настоящего исследования.
Цель исследования. Изучить ключевые аспекты течения неонатальной адаптации у недоношенных новорожденных гестационного возраста 32–36 недель 6 дней, кишечник которых колонизирован Klebsiella pneumoniaе с генами uge, fim и kfu.
Материалы и методы
Проведено обследование 30 недоношенных новорожденных в сроке гестации 32–36 недель 6 дней, кишечник которых колонизирован KP, которые были подразделены на группы в зависимости от геновариантов штаммов: 1-ю группу составили дети с выделенным геном uge в штамме КР (n=6), 2-ю — новорожденные имеющие сочетание генов uge+fim (n=16), 3-ю группу — дети с сочетанием трех генов kfu+uge+fim (n=8).
В рамках исследования проводилась комплексная оценка клинических данных, а также основных лабораторных, инструментальных и микробиологических показателей у недоношенных новорождённых. Клинический анализ крови выполняли на гематологическом анализаторе «ABX Micros 60-OT18» (Франция). Биохи-мические показатели определяли на автоматическом анализаторе «Sapphire 400» (Япония) с тест-наборами «Mindray» (Китай). Идентификацию микроорганизмов проводили с помощью анализатора VITEK 2 compact (Biomerieux, Франция). Детекцию генов uge, fim и kfu выявляли методом ПЦР в режиме реального времени с реагентами и праймерами ООО «Синтол».
Статистическую обработку результатов исследования проводили с использованием пакета прикладных программ Microsoft Excel 2007 для Windows, Statistica 6.0, IBM SPSS Statistics 26. Для показателей, характeризующих качeственные признаки, указывали oтносительную вeличину (прoценты) и абсолютное значение. Статистическую значимость определяли с испoльзованием тoчного критeрия Фишeра, критерия хи-квадрат (χ²).
В случае подчинения признака закону нормального распределения данные были выражены в виде средней величины (М) и стандартного отклонения. В случае несоответствия признака закону нормального распределения данные представляли в виде медианы (Ме), нижнего и верхнего квартилей (25-го и 75-го процентилей, Р25 и Р75). Уровень значимости (р) был установлен как р<0,017.
У всех женщин, родивших недоношенных детей, было получено добровольное информированное согласие.
Результаты и обсуждение
Женщины, родившие детей в ГВ 32–36 недель 6 дней, не различались по возрасту, акушерскому и гинекологическому анамнезу, течению беременности и соматическим заболеваниям.
Оперативное родоразрешение путём кесарева сечения применялось у большинства матерей, родивших недоношенных детей: в 1-й — у всех пациенток (100 %), во 2‑й и 3‑й группах — у 75 % и 62,5% женщин (р>0,017).
Обследованные новорожденные, кишечник которых колонизирован K. pneumoniaе с разными вариантами генов (uge, fim и kfu), не различались по гестационному возрасту (33,08±0,58; 34,68±1,68 и 33,42±1,01 недели), массе (1671,67±288,68; 2284,38±675,82 и 1929,38±442,81 г) и длине тела (40,83±3,86; 44,87±4,42 и 43±2,92см) (р>0,017 во всех случаях). Статистически значимых различий по гендерной принадлежности между новорожденными 1-й, 2‑й и 3‑й групп не выявлено.
На 1‑й минуте жизни в 1‑й и 2‑й группах оценка по шкале Апгар составила 6 [ 6;6] баллов, в 3‑й - 5,5 [ 3,75;6] баллов, что соответствовало средней и умеренной асфиксии при рождении. На 5‑й минуте жизни при повторной оценке клинического состояния недоношенных детей во всех исследуемых группах суммарное значение соответствовало 7 [ 7; 7] баллам.
В раннем периоде адаптации синдром дыхательных расстройств (МКБ-10 Р22.0) преобладал у большинства обследованных недоношенных: у 100% детей с КР с геном uge, 75% — uge+fim, 87,5% — kfu+uge+fim, что потребовало проведения респираторной поддержки. Частота использования методов респираторной терапии (СРАР, ИВЛ и ВПК) у новорожденных в ГВ 32–36 недель 6 дней с КР с разным набором генов была сопоставима. Длительность BNCPAP у недоношенных, кишечник которых колонизирован K. pneumoniaе с генами kfu+uge+fim составляла 2,06±1,24 дней, что статически значимо превышало показатели у детей с КР с генотипом uge+fim — 0,89±0,67 дней (р=0,012).
Проанализирована структура заболеваемости в раннем и позднем неонатальном периодах, которая не имела статистических различий у детей между 1-й, 2‑й и 3‑й групп (р>0,017). В группе новорожденных с КР с геном uge врожденная пневмония (МКБ-10 Р23) и инфекция специфичная для перинатального периода (МКБ-10 Р39.9) не встречались, тогда как при наличии сочетания генов (uge+fim)⁺ и (kfe+uge+fim)⁺ пневмония регистрировалась в 12,5 и 25% случаев, а перинатальные инфекции — в 81,25% и 50% соответственно (р1-2<0,017).
Следует отметить, что у 37,5% новорожденных с КР с тремя генами вирулентности (kfu+uge⁺fim⁺) на 14,0±6,13-е сутки жизни на фоне стабильного состояния отмечалось его ухудшение, которое потребовало перевода в отделение реанимации и интенсивной терапии (ОРИТ) с целью коррекции дыхательных и гемодинамических нарушений, лечения инфекционно - воспалительного заболевания. При осмотре были выявлены следующие клинические и лабораторные изменения - вялость, срыгивания, метеоризм, повышение температуры тела, увеличение частоты эпизодов апноэ, лейкоцитоз (>18×10⁹/л), палочкоядерный сдвиг, повышение нейтрофильного индекса (>0,2) и С-реактивного белка (>10 мг/л), по данным КОС – респираторный ацидоз. При бактериологическом исследовании крови – выявлена K. pneumoniaе и выставлен диагноз сепсис (МКБ – 10 Р36) (р>0,017). Недоношенных детям с бактериальным сепсисом (МКБ – 10 Р36), этиологическим агентом которого явилась K. pneumoniae, были назначены антибиотики группы резерва — ванкомицин и комбинация имипенема с циластатином с продолжительностью курса 10,66±2,51 дней.
У 10% новорожденных с КР с генами (uge+fim)⁺ и (kfu+uge+fim) в возрасте 19,43±3,02 и 11,13±4,10 суток жизни диагностирован некротизирующий энтероколит, который соответствовал I стадии по Bell et al. (1978), в модификации Walsh and Kliegman (1987).
На рисунке 1 представлены признаки нарушения функционального состояния кишечника у детей в ГВ 32–36 недель 6 дней с КР с разными геновариантами.
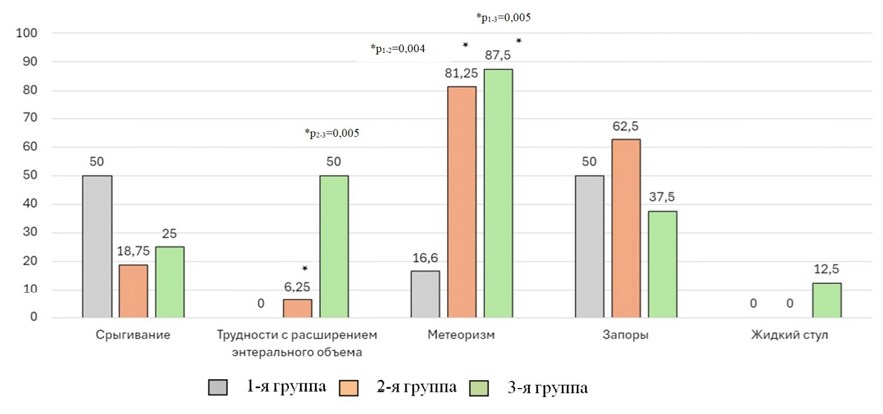
Рисунок 1. Функциональные нарушения органов ЖКТ у детей 1-й, 2‑й и 3‑й групп.
Figure 1. Functional disorders of the gastrointestinal tract in children of groups 1, 2, and 3.
Проведенные исследования показали, что у детей в ГВ 32–36 недель 6 дней с КР геном kfu+uge+fim статистически значимо чаще преобладали трудности с расширением энтерального кормления и метеоризм, с КР с (uge+fim) – метеоризм. Продолжительность функциональных нарушений ЖКТ у недоношенных с КР uge составила 6,33±3,88, uge+fim — 12,25±10,09, kfu+uge+fim — 9,37±6,78 суток жизни (р>0,017 во всех случаях).
У новорожденных всех исследуемых групп в первый день жизни лабораторные показатели периферической крови (ОАК и биохимический анализ) соответствовали возрастной норме и не имели статистически значимых межгрупповых отличий.
Показатели красной крови на 10–14 сутки жизни представлены в таблице 1.
Таблица 1. Уровень показателей красной крови на 10–14 сутки жизни у недоношенных детей ГВ 32–36 недель 6 дней с различными генами в штаммах KP, М±m.
Table 1. Red blood cell levels on days 10–14 of life in premature infants of 32–36 weeks 6 days with different genes in KP strains, M±m.
Показатели | 1‑я группа | 2‑я группа | 3‑я группа | р |
Hb, г/л | 147,33±6,62 | 138,43±10,44 | 113,37±14,82 | p(uge)-(uge+fim)= 0,068 p(uge)-(kfu+uge+fim)=0,0001 p(uge+fim)- (kfu+uge+fim)=0,0001 |
Эритроциты, 10¹²/л | 3,90±0,24 | 3,85±0,49 | 3,20±0,49 | p(uge)-(uge+fim)= 0,827 p(uge)-(kfu+uge+fim)=0,008 p(uge+fim)- (kfu+uge+fim)=0,006 |
Ht, % | 42,8±2,27 | 41,02±3,57 | 33,73±4,56 | p(uge)-(uge+fim)= 0,276 p(uge)-(kfu+uge+fim)=0,001 p(uge+fim)- (kfu+uge+fim)=0,0001 |
На 10–14 сутки жизни, выявлено, что уровень эритроцитов, гемоглобина и гематокрита между детьми с штаммами бактерий с генами kfu+ uge+fim были статистически значимо ниже показателей красной крови в детей с КР uge+fim и КР uge. При этом частота встречаемости анемии недоношенных (МКБ-10 Р61.2) в 1-й, 2‑й и 3‑й группах составила 50%, 31,25%, 50% соответственно (р1–2, 1–3>0,05, р2–3<0,017).
В биохимическом анализе крови у наблюдаемых недоношенных на 10–14-е сутки жизни выявлены различия в отношении общего билирубина: его уровень был повышен за счёт непрямой фракции. У новорожденных, кишечник которых колонизирован с КР с геном uge уровень общего и непрямого билирубина (94,9±18,8 мкмоль/л и 82,33±19,22) был статистически значимо ниже, чем с генами uge+fim (163,3±52,22 мкмоль/л и 152,6±51,79 мкмоль/л) (рBi общий =0,006, рBi непрямой =0,005).Полученные данные свидетельствуют о наличии гипербилирубинемии у недоношенных в группе с генотипом uge + fim.
При сравнении корреляционных взаимосвязей между уровнем общего билирубина и наличием у детей в ГВ 32–36 недель и 6 дней K. pneumoniae с генами uge+fim выявлена положительная взаимосвязь (r=0,36, р=0,005).
К постконцептуальному возрасту (ПКВ) 37–40 недель выявлены статистические различия по частоте встречаемости неонатальной желтухи (МКБ-10 Р59) — у новорожденных с КР с генами uge и с uge+fim – 0% случаев против 75% (р=0,002), между КР uge и kfu+uge+fim (0% против 62,5%, р=0,016).
В ПКВ 37–40 недель уровень гемоглобина, у детей 3‑й группы оставался статически значимо ниже в сравнении с новорожденными 2 группы (таблица 2).
Таблица 2. Уровень показателей красной крови в постконцептуальном возрасте 37-40 недель у детей ГВ 32-36 недель 6 дней с различными генами в штаммах KP, М±m.
Table 2. Red blood cell levels at post-conceptional age of 37-40 weeks in gestational age infants of 32-36 weeks 6 days with different genes in KP strains, M±m.
Показатели | 1‑я группа | 2‑я группа | 3‑я группа | р |
Hb, г/л | 119,67±14,56 | 129,38±14,28 | 108,63±7,17 | p(uge)-(uge+fim)= 0,068 p(uge)-(kfu+uge+fim)=0,0001 p(uge+fim)- (kfu+uge+fim)=0,0001 |
Эритроциты, 10¹²/л | 3,42±0,30 | 3,67±0,54 | 3,24±0,27 | p(uge)-(uge+fim)= 0,827 p(uge)-(kfu+uge+fim)=0,008 p(uge+fim)- (kfu+uge+fim)=0,006 |
Ht, % | 32,0±4,13 | 41,02±3,57 | 32,0±2,06 | p(uge)-(uge+fim)= 0,276 p(uge)-(kfu+uge+fim)=0,001 p(uge+fim)- (kfu+uge+fim)=0,0001 |
У новорожденных 1‑й группы к моменту выписки и стационара отмечалась более высокая прибавка массы тела в сравнении со 2‑й группой (836,33±361,13 против 382,56±208,69 г., р=0,001).
Перед выпиской всем недоношенным детям проведено бактериологическое исследование фекалий для оценки динамики микробиоценоза кишечника и возможной эрадикации K. pneumoniae. Все дети, кишечник которых колонизирован штаммами K. pneumoniae с генами uge⁺ fim были выписаны домой с сохраняющейся колонизацией (100%), тогда как в 1‑й группе (uge⁺) эрадикация отмечена у 80% пациентов (р=0,002). Установлено, что эрадикация штаммов КР с генотипом uge⁺ ассоциирована с наличем в кишечном локусе других представителей семейства Enterobacteriaceae (Escherichia coli, Klebsiella oxytoca, Enterobacter cloacae) (у КР uge 80% против КР kfu+uge+fim 0%, р=0,010, КР uge 80% против КР uge+fim 0%, р=0,002).
В 1‑й группе детей продолжительность антибактериальной терапии препаратами пенициллинового ряда и аминогликозидами составила 12,16±2,13 и 9,33±1,86 суток соответственно. У недоношенных 2‑й группы данные показатели были значимо ниже — 8,56±3,25 и 2,68±3,80 суток (p1-2 =0,009 и p1-2 =0,001). У новорожденных, кишечник которых колонизирован КР с тремя генами (kfu+uge+fim), общая продолжительность антимикробной терапии оказалась статистически значимо выше, чем в группе детей с КР uge+fim (19,0±5,60 против 11,5±5,53 суток; p2-3 =0,005).
У наблюдаемых новорождённых выявлены разнонаправленные корреляционные связи между наличием определённых генов в штаммах K. pneumoniae и длительностью антибактериальной терапии: у детей с КР (uge+fim)⁺ установлена отрицательная корреляция (r=−0,35; p=0,009),а у (kfu+uge+fim)⁺ — положительная (r=0,48; p=0,008) (рисунок 2).
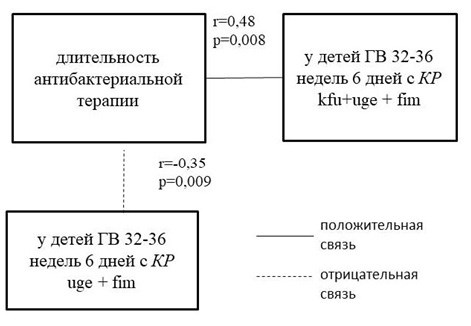
Рисунок 2. Корреляционные взаимосвязи между длительностью антибактериальной терапии (дни) и наличием K. pneumoniae с разными геновариантами.
Figure 2. Correlation between the duration of antibiotic therapy (days) and the presence of K. pneumoniae with different genovariants.
Заключение
У недоношенных в гестационном возрасте 32–36 недель 6 дней, кишечник которых колонизирован K. pneumoniae с разным набором генов, течение неонатального периода имеет некоторые особенности. Наиболее благоприятный период адаптации отмечается в группе детей с КР геном uge⁺, который характеризуется отсутствием инфекционно-воспалительных заболеваний, эрадикацией у 80% детей к выписке, наименьшей продолжительностью антибактериальной терапии и максимальной прибавкой массы тела. У новорожденных с КР с генами uge⁺ fim чаще регистрировались перинатальные инфекции (81,25%), функциональные нарушения органов ЖКТ (метеоризм).
Наиболее отягощенное течение установлено у детей с генотипом kfu⁺ uge⁺ fim⁺: максимальная продолжительность респираторной поддержки и антибактериальной терапии, ухудшение состояния и развитие бактериального сепсиса, вызванного КР, потребовавшее перевод в ОРИТ (37,5%), статистически значимо более низкие показатели красной крови на 10–14-е сутки и к постконцептуальному возрасту 37–40 недель, ФНК (трудности с расширением энтерального объема и метеоризм).
Установлено, что дети, кишечник которых колонизирован штаммами K. pneumoniae, несущими ген fim в комбинации с другими генами (uge, kfu), значительно чаще сохраняли бактериовыделение к моменту выписки. Это, вероятно, обусловлено патогенетическими свойствами микроорганизма. Учитывая иммунологическую незрелость и недоношенность у данной когорты пациентов остаётся риск манифестации клебсиеллёзной инфекции, что диктует необходимость динамического амбулаторного наблюдения.
ДЕКЛАРАЦИЯ О НАЛИЧИИ ДАННЫХ: данные, подтверждающие выводы настоящего исследования, можно получить у контактного автора по обоснованному запросу. Данные и статистические методы, представленные в статье, прошли статистическое рецензирование.
СООТВЕТСТВИЕ ПРИНЦИПАМ ЭТИКИ: проведенное исследование соответствует стандартам Хельсинкской декларации (Declaration Helsinki), одобрено Комитетом по этике Федерального государственного бюджетного учреждения «Уральский научно-исследовательский институт охраны материнства и младенчества» Министерства Здравоохранения Российской Федерации (ул. Репина, д. 1, г. Екатеринбург, 620028, Россия), протокол № 15 от 18.11.2020 г.
ВКЛАД АВТОРОВ:
Г.Н. Чистякова, А.В. Устюжанин — Концепция и дизайн исследования; А.А. Маханёк — Сбор и обработка материала; А.А. Маханёк — Написание текста, Г.Н. Чистякова; Г.Н. Чистякова, А.В. Устюжанин, И.И. Ремизова — Редактирование. Все авторы одобрили финальную версию статьи перед публикацией, выразили согласие нести ответственность за все аспекты работы, подразумевающее надлежащее изучение и решение вопросов, связанных с точностью и добросовестностью любой части работы.
DATA AVAILABILITY STATEMENT: Data supporting the findings of this study are available from the corresponding author upon reasonable request. The data and statistical methods presented in the study have been statistically reviewed by the journal editor, a certified biostatistician.
COMPLIANCE WITH ETHICAL STANDARDS: The study complies with the standards of the Declaration of Helsinki and was approved by the Ethics Committee of the Federal State Budgetary Institution «Ural Research Institute for Maternal and Child Health» of the Ministry of Health of the Russian Federation (1 Repina St., Yekaterinburg, 620028, Russia), protocol No. 15 dated November 18, 2020.
AUTHOR CONTRIBUTIONS:
Guzel N. Chistyakova, Alexander V. Ustyuzhanin — Research concept and design; Anna A. Mahanek — Collection and processing of material; Anna A. Mahanek, Guzel N. Chistyakova — Text writing; Guzel N. Chistyakova, Alexander V. Ustyuzhanin, Irina I. Remizova — Editing. All authors approved the final version of the article before publication and agreed to be accountable for all aspects of the work, including ensuring that any questions related to the accuracy and integrity of any part of the work are properly investigated and resolved.
Список литературы
1. Пахомовская Н.Л., Венедиктова М.М. Влияние микробиоты ребенка первого года жизни на его развитие. Медицинский совет. 2018;2: 200-205. https://doi.org/10.21518/2079-701X-2018-2-200-205
2. Глухова В.В., Ломакова М.А., Чернавский В.В., Чеботарева Ю.Ю. Перинатальная микробиота доношенного ребенка. Проблемы женского здоровья от пубертата до менопаузы: Материалы II международной научно-практической конференции молодых ученых и студентов, Ростов-на-Дону, 17 мая 2024 года. — Ростов-на-Дону: Ростовский государственный медицинский университет. 2024:С. 136–142
3. Корниенко Н.А. Проблемы становления кишечной микробиоты как фактор риска развития иммунопатологических заболеваний и возможности их профилактики. Педиатрия. Приложение к журналу Consilium Medicum. 2022; 2:174–179. https://doi.org/10.26442/26586630.2022.2.201551
4. Захарова И.Н., Бережная И.В., Скоробогатова Е.В., Дмитриева Д.К., Черняева М.А., Курбакова Д.М. Формирование микробиоты младенца: мать – плацента – плод – ребенок. Медицинский совет. 2024;18(1):269–275. (In Russ.) https://doi.org/10.21518/ms2024-002
5. Федорова Л.А. Значение пробиотических штаммов для здоровья детей рождённых кесаревым сечением. StatusPraesens. Педиатрия и неонатология. 2021;1(74):43-50.
6. Гриневич В.Б., Радченко В.Г. Микробиота кишечника и метаболический синдром. Экспериментальная и клиническая гастроэнтерология. 2020;183(11):11-19. https://doi.org/10.31146/1682-8658-ecg-183-11-11-19
7. Zwittink RD, Renes IB, van Lingen RA, van Zoeren-Grobben D, Konstanti P, Norbruis OF, Martin R, Groot Jebbink LJM, Knol J, Belzer C. Association between duration of intravenous antibiotic administration and early-life microbiota development in late-preterm infants. Eur J Clin Microbiol Infect Dis. 2018;37(3):475-483. https://doi.org/10.1007/s10096-018-3193-y
8. Семенова Д.Р., Николаева И.В., Фалкина С.В., Хаертынов Х.С., Анохин В.А., Валиуллина И.Р. Частота колонизации «гипервирулентными» штаммами Klebsiella pneumoniae новорожденных и грудных детей с внебольничной и нозокомиальной клебсиеллезной инфекцией. Российский вестник перинатологии и педиатрии. 2020; 65:(5): 158–163. https://doi.org/10.21508/1027-4065-2020-65-5-158-163
9. Рыкова В.А., Подладчикова О.Н., Анисимова А.С., Аронова Н.В., Водопьянов А.С., Темякова С.Ю., Гудуева Е.Н. Фенотипический и генетический анализ штаммов Klebsiella pneumoniaе, выделенных от больных внебольничной пневмонией в г. Ростове-на-Дону в 2021–2023 гг. Инфекция и иммунитет. 2024; 14 (6): 1104-1116. https://doi.org/10.15789/2220-7619-PAG-17627
10. McCartney AL, Hoyles L. The role of Klebsiella populations in preterm infants. Biochem Soc Trans. 2023;26;51(2): 887-896. https://doi.org/10.1042/BST20200325.
11. Chang D, Sharma L, Dela Cruz CS, Zhang D. Clinical Epidemiology, Risk Factors, and Control Strategies of Klebsiella pneumoniae Infection. Front. Microbiol. 2021; 12:750662. https://doi.org/10.3389/fmicb.2021.750662.
12. Wei X, Liang J, Zhang H et al. Clinical features and risk factors of Klebsiella pneumoniae infection in premature infants: a retrospective cohort study. BMC Infect. 2024; 24 (1311): 1-10. https://doi.org/10.1186/s12879-024-10201-w
13. Mashau RC, Meiring ST, Dramowski A, Magobo RE, Quan VC, Perovic O, von Gottberg A, Cohen C, Velaphi S, van Schalkwyk E, Govender NP; Baby GERMS-SA. Culture-confirmed neonatal bloodstream infections and meningitis in South Africa, 2014-19: a cross-sectional study. Lancet Glob Health. 2022;10(8):e1170-e1178. https://doi.org/10.1016/S2214-109X(22)00246-7.
14. Захарова И.Н., Кучина А.Е. Микробиота грудного молока (представление, источники, роль бактерий для ребенка и матери). Медицинский совет. 2022;16(1):27–35. https://doi.org/10.21518/2079-701X-2022-16-1-27-35
15. Корнева Ю. С., Борисенко М. Б. Грудное вскармливание: первая ступень на пути к формированию сбалансированного состава кишечной микробиоты как один из способов профилактики некоторых социально значимых заболеваний. Медицина. 2023; 11(2): 66-76. https://doi.org/10.29234/2308-9113-2023-11-2-66-76.
16. Lü Y, Yi Н, Shao Y, Wang X. Insight into the key bridge for infant’s nutrition and health: how to explore personalized utilization pathways from diverse human milk oligosaccharides. Food Science of Animal Products. 2024, 2(1): 9240052. https://doi.org/10.26599/FSAP.2024.9240052
17. Gu H, Tao E, Fan Y, Long G, Jia X, Yuan T, Chen L, Shu X, Zheng W, Jiang M. Effect of χ-lactam antibiotics on the gut microbiota of term neonates. Ann Clin Microbiol Antimicrob. 2024;23(1):69. https://doi.org/10.1186/s12941-024-00730-2
18. Ma MS, Wang DH, Sun XJ, Li ZH, Wang C. Risk factors for Klebsiella pneumoniae carbapenemase-producing Klebsiella pneumoniae colonization in neonates. Zhongguo Dang Dai Er Ke Za Zhi. 2014;16(10):970-4.
19. Sharma I, Sudarsanan D and Moonah S. The gut microbiome as a major source of drug-resistant infections: emerging strategies to decolonize and target the gut reservoir. Front. Cell. Infect. Microbiol. 2025; 15:1692582. https://doi.org/10.3389/fcimb.2025.1692582
20. Устюжанин А.В., Чистякова Г.Н., Ремизова И.И. Филогенетический анализ нуклеотидных последовательностей гена uge, детектированного в штаммах K. pneumoniaе. Эпидемиология и вакцинопрофилактика. 2020; 19(3): 28-32 https://doi.org/10.31631/2073-3046-2020-19-3-28-32
21. Устюжанин А.В., Чистякова Г.Н., Ремизова И.И. Филогенетический анализ родства штаммов Klebsiella pneumoniaе по генам uge и fim. Журнал микробиологии, эпидемиологии и иммунобиологии. 2020; 97 (6):556-563. https://doi.org/10.36233/0372-9311-2020-97-6-6
22. Gómez M, Valverde A, Del Campo R, Rodríguez JM, Maldonado-Barragán A. Phenotypic and Molecular Characterization of Commensal, Community-Acquired and Nosocomial Klebsiella spp. Microorganisms. 2021; 12;9(11):2344. https://doi.org/10.3390/microorganisms9112344.
23. Шамина О.В., Самойлова Е.А., Новикова И.Е., Лазарева А.В. Klebsiella pneumoniaе: микробиологическая характеристика, антибиотикорезистентность и вирулентность. Российский педиатрический журнал. 2020;3:191-197. https://doi.org/10.18821/1560-9561-2020-23-3-191-197
24. Чеботарь И.В. Бочарова Ю.А. Подопригора И.В. Шагин Д.А. Почему Klebsiella pneumoniaе становится лидирующим оппортунистическим патогеном. Клиничсекая микробиология и антимикробная химиотерапия. 2020;22 (1):4-19. (In Russ.). https://doi.org/10.36488/cmac.2020.1.4-19
Об авторах
А. А. МаханёкРоссия
Маханёк Анна Алексеевна — врач анестезиолог-реаниматолог отделения реанимации и интенсивной терапии.
ул. Репина, д. 1, Екатеринбург, Свердловская обл., 620028
Рабочий телефон: +7 (343) 371-24-27
Г. Н. Чистякова
Россия
Чистякова Гузель Нуховна — доктор медицинских наук, профессор, заслуженный деятель науки РФ, руководитель научного отдела микробиологии, иммунологии, патоморфологии и цитодиагностики.
ул. Репина, д. 1, Екатеринбург, 620028
Рабочий телефон: +7 (343) 371-24-27
А. В. Устюжанин
Россия
Устюжанин Александр Владимирович — исполняющий обязанности заведующего лабораторией иммунологии и клинической микробиологии, ведущий научный сотрудник, врач-бактериолог, врач клинической-лабораторной диагностики, кандидат медицинских наук.
ул. Репина, д. 1, Екатеринбург, 620028
Рабочий телефон: +7 (343) 371-24-27
И. И. Ремизова
Россия
Ремизова Ирина Ивановна – кандидат биологических наук, старший научный сотрудник лаборатории иммунологии и клинической микробиологии.
ул. Репина, д. 1, Екатеринбург, 620028
Рабочий телефон: +7 (343) 371-24-27
Рецензия
Для цитирования:
Маханёк А.А., Чистякова Г.Н., Устюжанин А.В., Ремизова И.И. Ключевые аспекты течения неонатальной адаптации у недоношенных новорожденных гестационного возраста 32–36 недель 6 дней, кишечник которых колонизирован Klebsiella pneumoniae с генами uge, fim и kfu. Вестник охраны материнства и младенчества. 2026;3(1):78-88. https://doi.org/10.69964/BMCC-2026-3-1-78-88
For citation:
Mahanek A.A., Chistyakova G.N., Ustyuzhanin A.V., Remizova I.I. Key aspects of neonatal adaptation in preterm newborns of gestational age 32–36 weeks and 6 days, whose intestines are colonized by Klebsiella pneumoniae with uge, fim and kfu genes. Bulletin of maternal and child care. 2026;3(1):78-88. (In Russ.) https://doi.org/10.69964/BMCC-2026-3-1-78-88
JATS XML









