Перейти к:
Оценка эффективности ведения беременных из группы критических акушерских состояний в стратегии снижения материнской смертности
https://doi.org/10.69964/BMCC-2025-2-5-82-93
Аннотация
Введение. В Российской Федерации (РФ) в 2021 году приказом Минздрава России утвержден Регламент и мониторинг критических акушерских состояний (КАС), осуществляющий внесение пациенток с КАС в специализированную систему, и определена его роль в акушерской практике.
Цель. Доказать эффективность ранней диагностики и маршрутизации критических акушерских состояний в снижении показателя материнской смертности от акушерских кровотечений, преэклампсии и септических осложнений (от COVID-19) в условиях западной медицинской зоны Ханты-Мансийского автономного округа - Югра.
Материалы и методы. На первом этапе проведено исследование демографических показателей в Российской Федерации (РФ), Уральском Федеральном округе (УФО) и Ханты-Мансийском автономном округе (ХМАО) за последние 10 лет. На втором этапе проведено одноцентровое ретроспективное сравнительное исследование медицинской документации женщин в перинатальном центре (ПЦ) 3-го уровня. На третьем этапе в группу проспективного анализа, для оценки прогноза тяжелой ПЭ и определения сроков родоразрешения с учетом клиники ПЭ и показателей биохимического скрининга 1-го триместра, проведено исследование уровня ангиогенных факторов роста в 3 триместре беременности для определения прогноза тяжести ПЭ и сроков родоразрешения. Статистический анализ проводился с использованием программы Statistiсa 10 (США) и StatTech v. 2.8.4 (ООО «Статтех», Россия, 2020).
Результаты исследования. Структура КАС у беременных из медицинских организаций зоны ответственности перинатального центра ОКБ города Ханты-Мансийска в 2022 г. представлена в порядке убывания: ЭГЗ, в том числе заболеваниями, вызванными инфекцией SARS-CoV-2 (48,0 %), преэклампсией (31,3 %), акушерскими кровотечениями (11,2 %), септическими осложнениями (7,8 %). При этом в динамике за последнее десятилетие отмечено увеличение числа беременных, включенных в группу КАС с их маршрутизацией на родоразрешение в перинатальный центр города Ханты-Мансийска, что позволило за последние 9 лет не иметь случаев материнских потерь, в том числе от COVID-19 и ее осложнений. При этом число родов, как и повсеместно в УФО и РФ, имеет тенденцию к снижению: за последние 10 лет на — 31,1 %. По данным с территории западной-медицинской зоны ХМАО индекс выживаемости составил 100 %, индекс смертности равен нулю, в том числе от инфекции SARS-CoV-2 и ее осложнений.
Заключение. Имеющийся ресурс перинатального центра в составе многопрофильной больницы ХМАО, несмотря на увеличение возраста реализации репродуктивной функции пациенток, число беременных с коморбидной патологий позволяет более эффективно оказывать специализированную медицинскую помощь. Мультидисциплинарный подход к оценке тяжести пациенток с КАС, в том числе на фоне коронавирусной инфекция, вызванной вирусом SARS-CoV-2, позволил не допустить летальных материнских исходов у пациенток закрепленной территории.
Ключевые слова
Для цитирования:
Васильковская Е.Н. Оценка эффективности ведения беременных из группы критических акушерских состояний в стратегии снижения материнской смертности. Вестник охраны материнства и младенчества. 2025;2(5):82-93. https://doi.org/10.69964/BMCC-2025-2-5-82-93
For citation:
Vasilkovskaya E.N. Evaluation of the effectiveness of care for pregnant women with critical obstetric conditions in the maternal mortality reduction strategy. Bulletin of maternal and child care. 2025;2(5):82-93. (In Russ.) https://doi.org/10.69964/BMCC-2025-2-5-82-93
Введение
В условиях спада рождаемости и отрицательного прироста населения страны одним из важных направлений политики государства на предполагаемую перспективу действий до 2030 года, является снижение коэффициента перинатальных потерь и сохранение репродуктивного здоровья женщин и детей [1,2,4,5].
В современных условиях продолжающегося демографического кризиса естественная убыль населения в России, по данным Росстата, в 2023 году составила 4,0 на 1000 населения, а суммарный коэффициент рождаемости был отрицательным –1,42 [6]. За этот же период времени демографические показатели Ханты-Мансийского автономного округа — Югры (ХМАО — Югра, ХМАО) показали, что естественная убыль населения в округе отсутствует, естественный прирост составил 4,7 на 1000 населения, однако, несмотря на это естественный прирост за последние 10 лет снизился. Суммарный коэффициент рождаемости составил 1,66, при этом и этот показатель в динамике также снижается [7].
Определено, что большие акушерские синдромы (БАС) являются основой критических акушерских состояний (КАС) и выступают в качестве основных предикторов риска материнской и младенческой заболеваемости и смертности [8]. К группе КАС в акушерской практике были отнесены акушерские кровотечения, тяжелая преэклампсия (ПЭ) и другие осложнения беременности [9-12]. При этом в структуре материнской смертности (МС) на первом месте, в порядке ранжирования стоят экстрагенитальные заболевания [13-15].
Патофизиология КАС глобально изучена с позиций функциональных систем [16]. В акушерской науке и практике благодаря работам R. Romero (2009) была принята концепция общности механизмов формирования тяжелых осложнений беременности, которая позволила взглянуть на роль плаценты и других провизорных органов с позиций плаценто-ассоциированных заболеваний [17]. К числу данных заболеваний, относится патология беременности, являющаяся причиной КАС [18-22]. При этом, на примере ПЭ, несмотря на то, что наши представления о природе и механизмах формирования данной патологии расширились, они далеки до окончательного понимания. Несмотря на это, появление ранних эффективных диагностических критериев и лечебных практик позволяет на будущее смотреть с некоторым оптимизмом [23-26].
Суммируя данные литературы об основных механизмах формирования ранней ПЭ, не вызывает сомнения тот факт, что в основе данного осложнения беременности лежит патология ангиогенеза и поверхностная инвазия цитотрофобласта в спиральные артерии матки, приводящая к нарушению плацентарной перфузии с последующим формированием ангиогенного дисбаланса и эндотелиальной дисфункции — избыточной продукции антиангиогенных факторов, и недостаточной продукции проангиогенных факторов, и факторов роста [26-29]. Типичным представителем антиангиогенных факторов является растворимая fms-подобная тирозинкиназа 1 (sFlt-1), а проангиогенных факторов — плацентарный фактор роста (PlGF) [26]. Комплексное исследование маркеров ангиогенеза — отношение растворимой fms-подобной тирозинкиназы 1 к плацентарному фактору роста, (sFlt-1/PlGF) совместно к общепринятым маркерам первого пренатального скрининга в рамках Фонда медицины плода или в III триместре беременности, при своевременной маршрутизации, позволяет прогнозировать развитие ПЭ тяжелой степени, и добиться улучшения перинатальных исходов [26-28]. Исторически сложилось, что исследование негативных факторов риска приводило к разработке конструктивных методов их устранения и профилактики. В связи с вышесказанным определена актуальность нашего исследования.
Цель — доказать эффективность ранней диагностики критических акушерских состояний и маршрутизации пациенток с КАС в снижении показателя материнской смертности от акушерских кровотечений, преэклампсии и септических осложнений (от COVID-19) в условиях западной медицинской зоны Ханты-Мансийского автономного округа- Югра.
Материалы и методы исследования
Настоящее исследование проведено в три этапа. На первом этапе проведена оценка демографических показателей в РФ, УФО, ХМАО за последние 10 лет.
На втором этапе проведено одноцентровое ретроспективное сравнительное исследование путем анализа медицинской документации пациенток, прошедших этап госпитализации и родоразрешения в Окружной клинической больнице (ОКБ) города Ханты-Мансийска, и имеющем в своем составе Перинатальный центр (ПЦ) 3-го уровня. Установлены три нозологические формы заболеваний — акушерские кровотечения, преэклампсия (ПЭ), и экстрагенитальная патология, обусловленная коронавирусной инфекцией (вызванной SARS-CoV-2), занимающие лидирующие позиции в структуре КАС. Для определения эффективности мониторинга КАС анализируемые случаи с массивными акушерскими кровотечениями и ПЭ были разделены на 2 группы сравнения: случаи, которые были родоразрешены в 2010-2011 годы (n=104; n=58) и случаи за 2019-2020 годы (n=81; n=74) соответственно. Выборка в каждом периоде времени формировалась сплошным способом. Случаи с коронавирусной инфекцией были проанализированы за периоды март 2020 г. — по апрель 2022 г. (в период эпидемии) и разделен на 2 группы сравнения — пациентки со среднетяжелым течением коронавирусной инфекцией из группы критических акушерских состояний и легким течением инфекции (n=25; n=123).
На третьем этапе проведено проспективное когорортное исследование для оценки прогноза тяжелой ПЭ и определения сроков родоразрешения на основании клиники ПЭ и показателей биохимического скрининга 1-го триместра, а также оценки уровня ангиогенных факторов роста — растворимой Fms-подобной тирозин-киназы-1 и плацентарного фактора роста (sFlt-1/PlGF) в 3 триместре беременности. В режиме реального времени обследованы пациентки с одноплодной беременностью и гипертензивными расстройствами, родоразрешенные в ПЦ г. Ханты-Мансийска (n=69). Анализируемые случаи были разделены на 3 группы сравнения: 1 группа (n=19) — беременные с ПЭ тяжелой (О14.1), 2 группа (n=32) — беременные с ПЭ умеренной и гестационной артериальной гипертензией (О13 О14.0) и 3 группа (n=17) — с гипертонической болезнью I-II стадии (O10.0) без ПЭ.
Статистический анализ проводили с помощью программного обеспечения Microsoft Office Excel 2021 (Microsoft, США и Statistica 10 (StatSoft, США), а также с использованием программы StatTech v. 2.8.4 (ООО «Статтех», Россия, 2020). Описание качественных показателей осуществлялось при помощи абсолютных значений и доли от целого; анализ статистической значимости различий качественных признаков, не соответствующих закону нормального распределения, выполнен методом углового преобразования Фишера. Описание полученных количественных результатов выполнен с использованием медианы (Ме) и интерквартильного интервала (Q1; Q3). Для оценки их различий использовали непараметрический U-критерий Манна — Уитни, результаты считали статистически значимыми при р< 0,05.
Результаты исследования и обсуждение
Эффективности внедрения системы оценки КАС в прогнозе и предупреждении случаев материнской и младенческой заболеваемости и смертности уделяется огромное внимание, и его использование в настоящий момент контролируется государством.
Территория ХМАО условно разделена на три медицинские зоны (западную, центральную, восточную) и обслуживается тремя перинатальными центрами 3-го уровня. Западная медицинская зона имеет свои особенности оказания перинатальной помощи: значительную удаленность медицинских организаций 1 и 2 уровня от перинатального центра, неравномерное распределение населения на территории.
Анализ структуры КАС в ХМАО представлен на рисунке 1. В структуре причин КАС в ХМАО лидирующие позиции занимает ПЭ, доля которой за три года возросла на 2,4 %, актуальными остаются акушерские кровотечения (почти на одном уровне с 2021 годом), отмечено увеличение частоты гнойно-септических осложнений (в 19,5 раза). Доля ЭГЗ после завершения эпидемии коронавирусной инфекции в 2022 году в ХМАО имела тенденцию к снижению.
В 2021 г. по отношению к 2020 г. по ХМАО количество случаев КАС повысилось в 16,2 раза, что можно объяснить эпидемиологическим процессом COVID-19 с вовлечением в эпидпроцесс беременных, рожениц и родильниц, а также обусловленная маршрутизацией пациенток в МО 3 уровня, при реализации трехуровневой системы оказания перинатальной помощи.
Динамика показателей индекса выживаемости и смертности в ХМАО после внедрения мониторинга пациенток с КАС представлена на рисунке 2.
Эффективность мониторинга беременных с КАС определяется за счет успешно решения несколько вопросов:
- масштабный охват консультированием беременных высокого риска;
- обеспечение своевременной маршрутизации пациенток с КАС в стационарные отделения МО 3 уровня;
- активный поиск анамнестических, клинических, лабораторных и инструментальных предикторов тяжести патологии, обусловленной заболеваниями и осложнениями гестации из перечня КАС;
- применение современных практик для лечения, при постоянно меняющихся критериях тяжести патологии, и своевременного определения показаний для родоразрешения и др.
В современных условиях при использовании предложенной стратегии более эффективно реализуются задачи предупреждения материнской и младенческой заболеваемости и смертности. По статистическим данным на рисунке 2 в ХМАО с 2020 года отмечен рост индекса выживаемости и снижение индекса смертности.
Структура КАС у беременных из медицинских организаций зоны ответственности перинатального центра ОКБ города Ханты-Мансийска в 2022 г. представлена в порядке убывания: ЭГЗ, в том числе заболеваниями, вызванными инфекцией SARS-CoV-2 (48,0%), преэклампсией (31,3%), акушерскими кровотечениями (11,2%), септическими осложнениями (7,8%). При этом в динамике за последнее десятилетие отмечено увеличение числа беременных, включенных в группу КАС с их маршрутизацией на родоразрешение в перинатальный центр города Ханты-Мансийска, что позволило за последние 9 лет не иметь случаев материнских потерь, в том числе от COVID-19 и ее осложнений. При этом число родов, как и повсеместно в УФО и РФ, имеет тенденцию к снижению: за последние 10 лет на — 31,1%. По данным с территории западной-медицинской зоны ХМАО индекс выживаемости составил 100%, индекс смертности равен нулю, в том числе от инфекции SARS-CoV-2 и ее осложнений.
Проведенный сравнительный анализ социально-демографических факторов у пациенток с массивными акушерскими кровотечениями показал, что возраст пациенток с акушерскими кровотечениями составил 28,1 (24,0 — 32,0) лет и 31,3 (28,0 — 35,0) лет, p=0,001, с увеличением его за последние 10 лет. Число беременных более 30 лет увеличилось в 6,5 раз — 2 (1,9%) и 10 (12,3%), p=0,001*. В 2019-2020 годах по отношению к пациенткам в 2010-2011 гг. отмечено увеличение их числа со средним (11,5/39,5%) и высоким риском кровотечений (1/8,6%), p=0,001 и p=0,03 соответственно. В порядке убывания кровотечения представлены такими причинами: раннее гипотоническое кровотечение (45,6%, -6,9%); задержка частей последа (21,0%; -16,0%); предлежание плаценты с кровотечением (17,3%; +80,2%); отслойка плаценты (16,0%; +28,0%) (р>0,05). Факторами риска развития послеродовых кровотечений в 2019-2020 годах послужили наличие одного рубца на матке — 22 (27,2 %), x2=8,54, p=0,01*, ОР=3,15 (ДИ 95 % [ 1,43-6,97]), 2-х и более рубцов — 8 (9,9 %), в 10 раз чаще, x2=7,82, p=0,01*, ОР=11,29 (ДИ 95 % [ 1,38-92,21]).
Родоразрешение путем операции кесарева сечения, по сравнению с предыдущим десятилетием в 2019-2020 гг. явилось вторым значимым фактором риска — у 31 (29,8%) и 50 (61,7%), x2=18,85, p=0,001*, ОР=3,80 (ДИ 95 % [ 2,05-7,02]). Доля массивных акушерских кровотечений увеличилась в 2,4 раза и выявлена у 7 (6,7%) и 13 (16,0%), р=0,05, ОР=2,65 (ДИ 95% [ 1,00-6,99]), при этом кровопотерю 4 ст. имели 3 (2,9%) и 6 (7,4%) пациенток, x2=2,01, р=0,05, ОР=2,65 (ДИ 95% [ 1,00-6,99]).
Фоном для развития акушерского кровотечения явилась железодефицитная анемия во время беременности — 56 (53,8%) и 55 (67,9%) x2=3,75, р>0,05, в их числе анемия средней и тяжелой степени — 8 (7,7%) и 7 (8,6%), x2=0,05, без статистически значимых отличий показателя; гестационный сахарный диабет (ГСГ) — у 1 (0,96%) и 23 (28,4%), x2=33,72, p=0,001*; вульвовагинит во время беременности — 4 (3,8%) и 18 (22,2%), р=0,001*, x2=14,67; артериальная гипертензия после 20 недель — у 25 (24,0%) и 3 (3,7%), x2=14,66, p=0,001*. Число случаев с артериальной гипертензии возникшей после 20 нед гестации в условиях современной диспансеризации беременных снизилось в 6,5 раз.
Путем операции кесарева сечения в группе пациенток с акушерскими кровотечениями были родоразрешены 31 (29,8%) и 50 (61,7%), x2=18,85, p=0,001*, ОР=3,80 (ДИ 95 % [ 2,05-7,02]), что также отразилось на частоте и массивности акушерского кровотечения.
В 2019–2020 по сравнению с 2010-2011 годом изменились медикаментозные и хирургические технологии остановки акушерских кровотечений. Эмболизация маточных артерий (ЭМА) была использована в 3 раза чаще (6,7/21%, p=0,002*); перевязка маточных артерий + гемостатические швы в 6,5 раза чаще (1,9/12,3%, p=0,011*). В группе женщин с ЭМА и комплексной терапией, остановки кровотечения удалось достигнуть остановки кровотечения у значительного большинства — 42/46 (91,31%) пациенток; неудачи составили 4/46 (8,69%) случаев, что потребовало выполнение гистерэктомии и требует дальнейшего совершенствования метода.
Таким образом, своевременная маршрутизация в перинатальный центр 3 уровня с наличием современных диагностических и лечебных технологий, в том числе ЭМА, позволила у пациенток высокого риска кровотечений добиться снижения показателя органоуносящих операций, а также материнской заболеваемости.
Проблема ПЭ является одним из основных факторов, угрожающим жизни пациенток в период гестации. Средний возраст пациенток при деторождении за последнее десятилетие имел статистически значимые отличия в сторону возрастания и составил 28,4 (24,0 — 33,0) и 31,7 (27,0 — 37,0), p=0,001*. При постановке на учет по беременности у пациенток с ПЭ вес составил 68,5 кг (57,0 — 73,0) и 71,1 кг (58,9 — 81,0), p=0,01, и соответственно ИМТ 26,2 (22,3 — 28,0) и 29,3 (24,9 — 33,3), p=0,001*.
Срок родов и масса плода у пациенток с ПЭ (медиана) составили 34,3 и 35,0 недель,; 2085,1 г. и 2365,6 г., p>0,05. При оценке состояния новорожденных у пациенток с ПЭ, наихудшие показатели имели дети, рожденные в 2010–2011 гг. по сравнению с 2019-2020 гг.: асфиксия — у 29 (50,0%) и 27 (37,5%), p=0,03*, более половины новорожденных имели задержку роста плода — 35 (60,3 %) и 40 (54,1 %) соответственно, без статистически значимых отличий; каждый 2-й ребенок был переведен в ОРИТН: 24 (41,4 %) и 17 (23,03 %), p=0,04*, на ИВЛ переведено на 13% больше новорожденных.
Прогнозирование тяжелой ПЭ с использованием маркеров пренатального скрининга первого триместра и sFlt-1/PlGF в 3 триместре беременности
При проспективном исследовании уровня sFlt-1/PlGF в 3 триместре беременности у пациенток с одноплодной беременностью и гипертензивными расстройствами, анализируемые случаи (n=69) были разделены на 3 группы сравнения: 1 группа (n=19) — беременные с ПЭ тяжелой (О14.1), 2 группа (n=32) — беременные с ПЭ умеренной и гестационной артериальной гипертензией (О13 О14.0) и 3 группа (n=17) — с гипертонической болезнью I-II стадии (O10.0) без ПЭ. В группе с тяжелой ПЭ выявлена максимальные цифры показателя — 187,63, p 1,2-3=0,001*, что в 7 раза чаще, чем в группе с АГ и в 2,5 раз чаще, чем в группе с умеренной ПЭ. В связи с полученными результатами пациентки с тяжелой ПЭ были родоразрешены в кратчайшие сроки от момента госпитализации: 3,79 (1,0–5,0) с., p1–2>0,05, p1–3=0,001*. При этом прогноз на развитие тяжелой ПЭ был также высоким как в группе с умеренной ПЭ, p1–2=0,001*, так и в группе с артериальной гипертензией без ПЭ, p1–3=0,001*.
Уровень протеинурии у пациенток с тяжелой ПЭ более 0,3 г/л выявлялся у 42,1 % беременных, менее 0,3 г/л — также у 42,1 % пациенток, p>0,05. При этом у 18,8 % беременных с умеренной ПЭ также выявлялась протеинурия более 0,3 г/л, p1–3=0,01*.
В наших исследованиях прогноз на развитие ПЭ тяжелой степени определялся на основании квартильного показателя sFlt-1/PlGF: 71,0 (у 31,6%) — 121,5 (у 21,1%) и был статистически значим (р=0,001*) по отношению ко всем другим группам исследования.
При использовании регрессионного анализа прогноз тяжелой ПЭ проведен на основании клиники ПЭ, показателей РАРРА, ХГЧ (скрининг 1 триместра), sFlt-1/PlGF в 3 триместре беременности. Все пациентки были разделены на 2 группы (таблица 1).
Среди биохимических маркеров пренатального скрининга 1 триместра только ХГЧ имел статистически значимые отличия между группами исследования. При этом соотношение уровня ангиогенного фактора к фактору роста плаценты (sFlt-1/PlGF) показала существенный рост показателя в группе с тяжелой ПЭ и его статистически значимые отличия (p<0,001*) от показателей у пациенток с диагнозами О14.0, О13, O10.0 (рисунок 3).
В продолжении исследования нами была проведена оценка зависимости вероятности диагноза (О14.1) от значения логистической функции P, которая показала, что площадь под ROC-кривой составила 0,84 ± 0,06 с 95% ДИ: 0,72 — 0,96 и она имела статистически значимые отличия от группы с умеренной ПЭ и артериальной гипертензией не связанной с беременностью, p<0,001*.
Дополнительно в исследовании была проведена проверка связи предикторов биохимического скрининга 1 триместра (ХГЧ) с вероятностью выявления тяжелой ПЭ. Результаты отражены в таблице 2.
Чувствительность и специфичность модели определения тяжелой ПЭ составили 78,9 % и 77,6 %, соответственно. Итоговый вклад всех факторов в модели тяжелой ПЭ — прогностическая значимость положительного результата — PVP составила 77,9 %, прогностическая значимость отрицательного результата — PVN составила 78,6 %.
Таким образом, показатели частоты ПЭ в округе за последнее десятилетие демонстрирует непрерывный рост что, по-видимому, связано с увеличением возраста реализации репродуктивной функции женщиной, увеличением массы и индекса массы тела, ростом заболеваемости ГСД и др. Современные диагностические технологии при своевременном родоразрешении, позволяют улучшить перинатальные исходы гестации.
Исходы беременности и родов у пациенток с коронавирусной инфекцией, вызванной вирусом SARS-CoV-2 в структуре КАС
Случаи с коронавирусной инфекцией с марта 2020 г. — по апрель 2022 г. (в период эпидемии) были разделены на 2 группы сравнения — пациентки со среднетяжелым течением коронавирусной инфекцией из группы критических акушерских состояний и легким течением инфекции (n=25; n=123).
Возраст пациенток в группах исследования не имел статистически значимых отличий и составил 31,9 (26,0 — 36,0) и 31,1 (27,0 — 35,0), p=0,57. ИМТ до беременности (кг/м2) составил 27,9 (23,0 — 32,9) и 24,8 (21,4 — 27,5), p=0,02 По результатам пренатальной диагностики 1-го триместра у пациенток с КАС в 5 раз были повышены риски ПЭ/ЗРП — 3/25 (12,0 %) и 3/123 (2,4%), x2=4,88, p=0,06; ОР=5,45 (95% [ 1,03-28,79]; признаки ПН выявлялись — у каждой второй беременной группы КАС — 12/25 (48,0%) и 34/123 (27,6%), x2=4,02, p=0,06; ОР=2,42 (95% [ 1,00-5,82]). Фоном для формирования ПН могли послужить средняя и тяжелая анемия в группе беременных с КАС выявлялась в 3,6 раз чаще — 3/25 (12,0%) и 4/123 (3,3%), x2=3,53, р>0,15, ОР=4,06 (95% [ 0,85-19,39]); ГСД выявлялся в 1,5 раза чаще — 9/25 (36,0%) и 30/123 (24,4%), x2=1,44, p>0,05; ОР=1,74 (95% [ 0,70-4,35]). В группе пациенток, входящих в КАС, все больные имели среднюю и тяжелую степень заболевания — 8/25 (32,0%), х2=0,13, p=0,82, ОР=0,84 (ДИ 95 % [ 0,34-2,12]); 17/25 (68,0%), х2=81,80, p=0,001*, ОР=128,56 (ДИ 95 % [ 25,18-656,53]). Тяжесть состояния в основном, кроме 4/25 (16%) беременных, была обусловлена осложненным течением пневмонии и тромбоэмболическими осложнениями. Перевод в ОРИТ имели 23/25 (92,0%) и 3/123 (2,4%) женщины, х2=115,08 p=0,001*, ОР=460,00 (ДИ 95 % [ 72,76-2908,05]), перевод на ИВЛ — у каждой второй беременной группы КАС — 11/25 (44,0%), х2=41,90, p=0,001*, ОР=31,43 (ДИ 95 % [ 7,82-126,37]); по отношению к пациенткам 2-й группы: 3/123 (2,4%) соответственно.
Результаты исходов беременности представлены в таблице 3.
Удельный вес пациенток с КАС при COVID-19 составил 25/148 (16,9 %) и имел высокие риски перинатальной заболеваемости. Таким образом, исходы гестации при заболевании инфицией SARS-CoV-2 в III триместре зависели от факторов риска (ожирения и ГСД) и качества оказания медицинской помощи. Тяжесть течения заболевания была сопряжена с развитием тяжелой пневмонии и ее осложнений, респираторного дистресса взрослых, сепсиса и органной дисфункции. Наиболее значимыми организационными мероприятиями в предотвращении перинатальных потерь была правильная маршрутизация всех беременных и родильниц в перинатальный центр 3 уровня и мультидисциплинарный подход к оказанию им медицинской помощи.

Рисунок 1. Структура причин критических акушерских состояний в ХМАО
Figure 1. The structure of the causes of critical obstetric conditions in the Khanty-Mansi Autonomous Okrug

Рисунок 2. Динамика показателей индекса выживаемости и смертности в ХМАО
Figure 2. Dynamics of the survival and mortality index in the Khanty-Mansi Autonomous Okrug
Таблица 1. Анализ уровня ХГЧ в зависимости от группы
Table 1. Analysis of hCG levels depending on the group
Показатель | Категории | Пренатальный скрининг 1 триместра — уровень ХГЧ | p | ||
Me | Q₁–Q₃ | n | |||
Группы | Диагноз (О14.1) | 46,82 | 40,16- 75,60 | 19 | 0,018* |
Диагноз (О14.0, О13, O10.0) | 35,71 | 27,24-54,86 | 49 | ||
* — здесь и далее влияние предиктора статистически значимо (p<0,05)
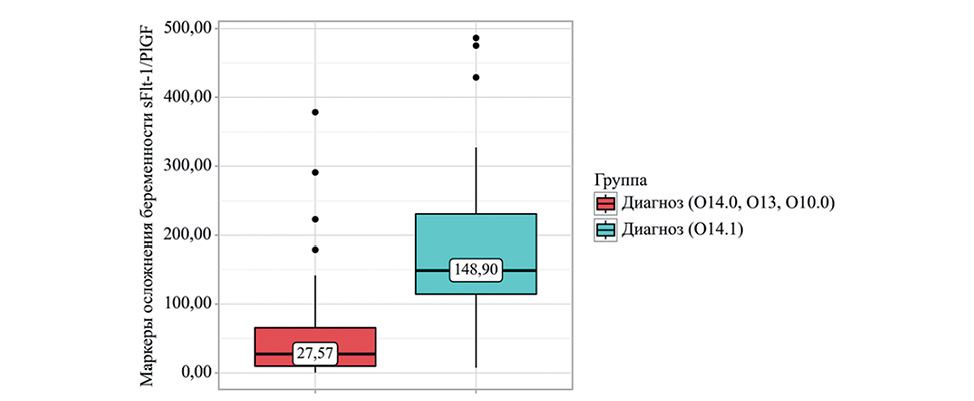
Рисунок 3. Показатель sFlt-1/PlGF в группе с тяжелой преэклампсией
Figure 3. sFlt-1/PlGF index in the group with severe preeclampsia
Таблица 2 — Связь предикторов биохимического скрининга 1 триместра (ХГЧ) с вероятностью выявления тяжелой преэклампсии
Table 2 — Association of predictors of first trimester biochemical screening (hCG) with the probability of detecting severe preeclampsia
Предикторы | Нескорректированный (Unadjusted) | Скорректированный (Adjusted) | ||
COR; 95% ДИ | p | AOR; 95% ДИ | p | |
Уровень ХГЧ | 1,023; 1,001 — 1,046 | 0,043* | 1,025; 0,998 — 1,052 | 0,070 |
Показатель sFlt-1/PlGF | 1,011; 1,004 — 1,017 | 0,001* | 1,010; 1,003 — 1,017 | 0,006* |
Таблица 3. Исходы беременности у пациенток с COVID-19; Me (Q1;Q3)
Table 3. Pregnancy outcomes in patients with COVID-19; Me (Q1;Q3)
Показатели/группы сравнения | Группа IIВ1, n=25 | Группа IIВ2, n=123 | p |
Медиана срока гестации, нед | 33.4 | 38.3 | p=0.001* |
Медиана массы новорожденного,г | 2236.9 | 3206.8 | p=0.001* |
Апгар на 1/5 мин, балл | 6.5 / 7.2 | 8.0 /8.4 | p=0.001* |
Заключение
Имеющийся ресурс перинатального центра в составе многопрофильной больницы ХМАО, при увеличении возраста реализации репродуктивной функции пациенток, числе беременных с коморбидной патологий позволяет более эффективно оказывать специализированную медицинскую помощь и создает возможность для предупреждения перинатальных потерь в акушерстве и неонатологии. Мультидисциплинарный подход к оценке тяжести пациенток с критическими состояниями, в том числе на фоне коронавирусной инфекция, вызванной вирусом SARS-CoV-2, позволил не допустить летальных материнских исходов у пациенток на закрепленной территории.
Список литературы
1. Регламент мониторинга критических акушерских состояний в Российской Федерации. — 2021. — URL: https://docs.cntd.ru/document/573626565/titles/6500IL (дата обращения: 18. 11. 2024).
2. Сухих Г.Т., Пугачев П.С., Артемова О.Р., Плутницкий А.Н., Шешко Е.Л., Прялухин И.А., Зарубина Т.В., Ашенбреннер И.В., Гойник Т.А., Кирпа-Иванов Т.А. Роль вертикально-интегрированной медицинской информационной системы по профилям «Акушерство и гинекология» и «Неонатология» в цифровой трансформации службы охраны материнства и детства. Национальное здравоохранение. 2021;2(3):18-28. doi: 10.47093/2713-069X.2021.2.3.18-28
3. Мурашко М.А., Сухих Г.Т., Пугачев П.С., Филиппов О.С., Артемова О.Р., Шешко Е.Л., Прялухин И.А., Гасников К.В. Международный и российский опыт мониторирования критических акушерских состояний. Акушерство и гинекология. 2021; 3: 5-11 doi: 10.18565/aig.2021.3.5-11
4. Филиппов О.С., Гусева Е.В. Материнская смертность в Российской Федерации в 2019 г.. Проблемы репродукции. 2020;26(6-2):8-26. doi: 10.17116/repro2020260628
5. Оленев А. С., Новикова В.А., Радзинский В.Е. Мировые концептуальные подходы к снижению материнской смертности. Акушерство и гинекология: новости, мнения, обучение. 2018;6 (3. Приложение.):5-17. doi: 10.24411/2303-9698-2018-13901
6. Здравоохранение в России. 2023 : статистический сборник. М.: Росстат, 2023;179 с.
7. Здоровье населения Ханты-Мансийского автономного округа ‒ по итогам 2022 года : статистические материалы / Бюджетное учреждение Ханты-Мансийского автономного округа — Югры «Медицинский информационно-аналитический центр». Ханты-Мансийск, 2023: 508 с.
8. Ковалев В.В., Кудрявцева Е.В., Миляева Н.М., Беломестнов С.Р. Большие акушерские синдромы: «гордиев узел» генных сетей. Уральский медицинский журнал. 2018;13 (168):40–47. doi: 10.25694/URMJ.2018.13.45
9. Воронова О. В. Морфогенез облитерационной ангиопатии в опорных ворсинах плацент беременных с преэклампсией : автореферат диссертации на соискание ученой степени кандидата медицинских наук. Москва, 2023. 25 с.
10. Оленев А.С., Вученович Ю.Д., Новикова В.А., Радзинский В.Е. Кровотечение как причина несостоявшейся и состоявшейся материнской смертности в условиях мегаполиса. Акушерство и Гинекология. Новости. Мнения. Обучение. 2019; 7 (3. Приложение.): 9–19. doi: 10.24411/2303-9698-2019-13901
11. Миляева Н.М., Багиянц В.А., Куликов А.В. Преждевременная отслойка нормально расположенной плаценты: морфологическая архитектура плаценты. Вестник охраны материнства и младенчества. 2025;2(4):61-69. doi: 10.69964/BMCC-2025-2-4-61-69
12. Щербак С.Г., Камилова Т.А., Голота А.С., Вологжанин Д.А. Факторы риска тяжелого течения и летального исхода COVID-19. Физическая и реабилитационная медицина, медицинская реабилитация. 2022; 4(1):14–36. doi: 10.36425/rehab104997
13. Мальгина Г.Б., Дьякова М.М., Бычкова С.В. и др. Новая коронавирусная инфекция в III триместре беременности: перинатальные и материнские последствия. Акушерство и гинекология. 2023; 4: 58–66. doi: 10.18565/aig.2023.58
14. Mullins E., Evans D., Viner R.M. et al. Coronavirus in pregnancy and delivery : rapid review. Ultrasound in Obstetrics and Gynecology. 2020;55(5): 586–592. doi: 10.1002/uog.22014
15. Petrilli C.M., Jones S.A., Yang J. et al. Factors associated with hospital admission and critical illness among 5279 people with coronavirus disease 2019 in New York City: prospective cohort study. BMJ. 2020;369:m1966. doi: 10.1136/bmj.m1966
16. Шанин В.Ю. Патофизиология критических состояний : монография. 3-е изд. Санкт-Петербург: ИП Макаров М.Ю., 2021. 440 с.
17. Romero, R. Prenatal medicine: the child is the father of the man. The Journal of Maternal-Fetal & Neonatal Medicine. 2009;22(8):636–639. doi: 10.1080/14767050902784171
18. Кудрявцева Е.В., Ковалев В.В., Угаров И.В. и др. Оценка роли некоторых генов-кандидатов в патофизиологии больших акушерских синдромов. Вестник уральской медицинской академической науки. 2019;16(4):432–449. doi: 10.22138/2500-0918-2019-16-4-432-449
19. Ives C.W., Sinkey R., Rajapreyar I. et al. Preeclampsia-Pathophysiology and Clinical Presentations: JACC State-of-the-Art Review. Journal of the American College of Cardiology. 2020; 76(14):1690–1702. doi: 10.1016/j.jacc.2020.08.014
20. Трифонова Е.А., Марков А.В., Зарубин А.А. и др. Анализ коэкспрессии генов плацентарного транскриптома как основа для поиска ключевых сигнальных путей и биомаркеров больших акушерских синдромов. Сибирский журнал клинической и экспериментальной медицины. 2021;36( 4):144–155. doi: 10.29001/2073-8552-2021-36-4-144-155
21. Brosens I., Puttemans P., Benagiano G. Placental bed research: I. The placental bed: from spiral arteries remodeling to the great obstetrical syndromes. American Journal of Obstetrics and Gynecology. 2019;221(5):437–456. doi: 10.1016/j.ajog.2019.05.044
22. Cornelius D. C. Preeclampsia: From Inflammation to Immunoregulation. Clinical Medicine Insights: Blood Disorders. 2018;11:1–6. doi: 10.1177/1179545X17752325
23. Кудрявцева Е.В., Ковалев В.В., Каюмова А.В. и др. Клинико-анамнестические особенности пациенток при неблагополучно завершенной гестации. Уральский медицинский журнал. 2019;183(15):36–42. doi: 10.25694/URMJ.2019.15.10
24. Сухих Г.Т., Тетруашвили Н.К., Трофимов Д.Ю. и др. Неинвазивный пренатальный ДНК-скрининг методом высокопроизводительного секвенирования у беременных с акушерской патологией. Доктор.Ру. 2017; 3 (132):11–15.
25. Андреева М.Д., Балаян И.С., Карахалис Л.Ю. Раннее прогнозирование преэклампсии: реальность сегодняшнего дня. Акушерство и Гинекология. Новости. Мнения. Обучение. 2023; 11(1):19–27. doi: 10.33029/2303-9698-2023-11-1-19-27
26. Башмакова Н.В., Цывьян П.Б., Чистякова Г.Н. и др. Ангиогенные ростовые факторы и патогенез преэклапсии. Российский вестник акушера-гинеколога. 2017;17(5):7-12. doi: 10.17116/rosakush20171757-12
27. Stepan H., Herraiz I., Schlembarch D., Verlohren S. et al. Inplementation of the sFlt-1/PlGF ratio for prediction and diagnosis of pre-eclampsia in singleton pregnancy: inplications for clinical practice. Ultrasound Obstet Gynecol. 2015; 45: 241-246. doi: 101002/uog.14799
28. Садыкова Г.К., Олина А.А. Роль матриксных металлопротеиназ в плацентарном ангиогенезе. Пермский медицинский журнал. 2021; 38(5):78–92. doi: 10.17816/pmj38578-92
29. Курцер М.А., Сичинава Л.Г., Алажажи А.О. и др. Ангиогенные факторы (sFlt-1, PlGF) у беременных с двойней и плацента-ассоциированными осложнениями. Акушерство, гинекология и репродукция. 2022;16 (5):541–551. doi: 10.17749/2313-7347/ob.gyn.rep.2022.330
Об авторе
Е. Н. ВасильковскаяРоссия
Елена Николаевна Васильковская, заместитель руководителя по акушерско-гинекологической помощи
628012; ул. Калинина, 40; 628911; ул. Мира, 40; Ханты-Мансийск
Тел.: +7 902 828-25-27, +73467390402
Рецензия
Для цитирования:
Васильковская Е.Н. Оценка эффективности ведения беременных из группы критических акушерских состояний в стратегии снижения материнской смертности. Вестник охраны материнства и младенчества. 2025;2(5):82-93. https://doi.org/10.69964/BMCC-2025-2-5-82-93
For citation:
Vasilkovskaya E.N. Evaluation of the effectiveness of care for pregnant women with critical obstetric conditions in the maternal mortality reduction strategy. Bulletin of maternal and child care. 2025;2(5):82-93. (In Russ.) https://doi.org/10.69964/BMCC-2025-2-5-82-93









