Перейти к:
Результаты электрокардиографии у детей, родившихся в сроке сверхранних преждевременных родов
https://doi.org/10.69964/BMCC-2024-1-1-117-129
Аннотация
Введение. Дети, рожденные в срок сверхранних преждевременных родов (СПР), составляют группу высокого риска развития сердечно сосудистых заболеваний, в том числе нарушений сердечного ритма (НСР) и проводимости в течение всей жизни.
Цель. Изучить электрокардиографические особенности у детей первого года жизни, рожденных в сроке СПР.
Материалы и методы. Основную группу составил 51 ребенок, рожденный в сроке СПР. В зависимости от массы тела основная группа была разделена на 2 подгруппы. 1 подгруппу составили дети с массой 500-750 г. (n=15). 2 подгруппу — дети с массой от 751 г. и более (n=36). В группу сравнения вошли 28 детей, родившихся в сроке гестации 32-36 недель. Обследование детей проводилось в возрасте 6 и 12 месяцев. Элетрокардиография проводилась детям в состоянии покоя в 12 стандартных отведениях со скоростью движения бумажной ленты 50 мм/сек. Анализ показателей ЭКГ проводился с помощью электрокардиографа «Сикард» Сименс АГ, по общепринятой методике.
Результаты и обсуждение. У детей, родившихся в сроке СПР в течение 1 года жизни наблюдались клинические проявления нарушения функционального состояния сердечно-сосудистой системы в виде вегето-сосудистой дисфункции, НСР, изменения характеристики сердечных тонов. По результатами ЭКГ были выявлены НСР в виде синусовой аритмии, синусовой тахи- и брадикардии, экстрасистолии, предсердного ритма, миграции водителя ритма, суправентрикулярной пароксизмальной тахикардии, WPW синдрома, синдрома удлиненного интервала QT, что составило у детей 1 подгруппы 86,7% случаев, у детей 2 подгруппы 82,2% и 60,7% у детей группы сравнения. Установлена прямая сильная корреляционная связь между клиническими проявлениями вегетативных дисфункций в возрасте 12 месяцев и частотой выявленных дисфункций. К 12 месяцам жизни увеличивается количество детей с синусовой брадикардией, синусовой аритмией и эктопическим ритмом. Положительной динамики в отношении частоты выявления ЭКГ-феноменов на протяжении первого года жизни не наблюдается.
Заключение. Детям, рожденным в сроке сверхранних преждевременных родов необходим кардиологический мониторинг, в том числе измерение артериального давления, проведения электрокардиографии и разработка персонифицированных программ диспансерного наблюдения.
Ключевые слова
Для цитирования:
Захарова С.Ю., Покусаева О.С. Результаты электрокардиографии у детей, родившихся в сроке сверхранних преждевременных родов. Вестник охраны материнства и младенчества. 2024;1(1):117-129. https://doi.org/10.69964/BMCC-2024-1-1-117-129
For citation:
Zakharova S.Yu., Pokusaeva O.S. Results of electrocardiography in children born at very early preterm birth. Bulletin of maternal and child care. 2024;1(1):117-129. (In Russ.) https://doi.org/10.69964/BMCC-2024-1-1-117-129
Введение
По оценкам Всемирной организации здравоохранения ежегодно до 15 миллионов детей рождаются преждевременно. Частота преждевременного рождения детей в мире колеблется от 5 до 10% [1]. Ведущее место в структуре заболеваемости взрослого населения занимает патология сердечно-сосудистой системы, рост которой начинается с детского возраста [2]. Сердечно-сосудистая система определяет функциональное состояние организма и его резервные возможности, а также степень адаптации к различным факторам внешней среды на всем протяжении жизни. Совершенно отчетливо проявляется прогрессирующий рост распространенности кардиологических заболеваний во всех возрастных группах и «омоложение» ряда заболеваний системы кровообращения [3].
Изучению состояния сердечно-сосудистой системы детей раннего возраста в популяции с учетом перинатального анамнеза, сроков и дефицита массы тела при рождении посвящены лишь единичные работы [2][4-10]. Факторы, приводящие к дефициту массы тела при рождении, способны стойко изменять структуру тела, нарушать метаболическую стабильность, снижать уровень адаптационных возможностей организма, реализующихся через деятельность эндокринной, иммунной, нервной и сердечно-сосудистой системы [6].
Неблагоприятные условия внутриутробного развития, постнатальные повреждения, в том числе и перинатальное поражение центральной нервной системы, как правило, нарушают процессы становления механизмов регуляции сердечно-сосудистой системы. Постгипоксическое поражение миокарда, по данным разных авторов [4-10], встречается у 15–50 % новорожденных с клиническими проявлениями церебральной ишемии. Гипоксическое повреждение клеток проводящей системы сердца может служить причиной нарушений сердечного ритма [4].
Неблагоприятное влияние перинатальной гипоксии проявляется развитием гемодинамических и метаболических нарушений в миокарде [5]. Особое значение приобретает патология беременности и родов, сопровождающаяся развитием острой или хронической гипоксии. Сочетанная гипоксия приводит к комбинированию различных видов аритмий [7]. Существующие исследования по электрокардиографическим показателям у недоношенных детей представлены различными данными [4-10]. Важную роль в формировании нарушений сердечного ритма играют и нарушения вегетативной регуляции [2][8-10].
Одним из ведущих патофизиологических механизмов развития аритмий в периоде новорожденности является нарушение нейрогенной регуляции сердечного ритма, приводящее к электрической нестабильности миокарда. Следствием этого является формирование различных нарушений ритма, которые манифестируют как в неонатальном периоде, так и в более старшем возрасте. Немаловажное значение в генезе аритмий имеет вегетативный дисбаланс, обусловленный повышением тонуса симпатической нервной системы [10].
Цель: изучить электрокардиографические особенности у детей первого года жизни, рожденных в сроке сверхранних преждевременных родов.
Материалы и методы
Проведено клинико-лабораторное обследование и наблюдение детей, родившихся в сроке сверхранних преждевременных родов, на протяжении первого года жизни.
Критерии включения: недоношенные дети первого года жизни, родившиеся в сроке 22 — 27,6 недель гестации, недоношенные новорожденные дети в сроке 32-36 недель гестации.
Критерии не включения: дети с хромосомными и генетическими заболеваниями, патологией обмена веществ, врожденными пороками сердца, дети с признаками СЗРП при рождении, заболеваниями почек и печени.
Основную группу составил 51 ребенок, рожденный в сроке сверхранних преждевременных родов. В зависимости от массы тела основная группа была разделена на 2 подгруппы. 1 подгруппу составили дети с массой 500-750 г (n=15). 2 подгруппу — дети с массой от 751 г и более (n=36). В группу сравнения вошли 28 детей родившихся в сроке гестации 32-36 недель. Достоверных различий по половому признаку между группами не было (p>0,05).
Набор материала проводился в центре мониторинга на базе ГАУЗ СО «Детская городская поликлиника №13» г. Екатеринбурга. Дети в возрасте 6 и 12 месяцев обследовались в амбулаторно-поликлинических условиях в ГАУЗ СО «Детская городская поликлиника №13» г. Екатеринбурга и в условиях дневного и круглосуточного стационара отделения детской реабилитации ФГБУ НИИ ОММ г. Екатеринбурга.
Изучение анамнестических данных проводилось на основании анализа медицинской документации: выписки из отделений патологии новорожденных, родильных домов, истории развития ребенка (ф. 112/у).
Параметры физического развития детей при рождении оценивали согласно полу с использованием диаграмм INTERGROWTH-21st (Международный консорциум по росту плода и новорожденного) [11]. Физическое развитие в возрасте 6 и 12 месяцев оценивали с учётом скорригированного возраста с помощью оценочных таблиц ВОЗ [12].
Элетрокардиография (ЭКГ) проводилась детям в состоянии покоя в 12 стандартных отведениях со скоростью движения бумажной ленты 50 мм/сек. Анализ показателей ЭКГ проводился с помощью электрокардиографа «Сикард» Сименс АГ, по общепринятой методике. Программа ЭКГ-исследования детей включала 3 стандартных, 3 однополюсных от конечностей и 6 однополюсных грудных отведения. При анализе ЭКГ кривых учитывалась продолжительность интервала QT, положение сегмента ST и амплитуда зубца Т.
Статистическая обработка данных проводилась с применением пакета программ Microsoft Excel «Statistica 10.0» и программы SPSS.23. Количественные показатели представлены в виде M±m, где M — среднее арифметическое, m — ошибка средней, а также в виде медианы (Мe) и значений верхнего и нижнего квартилей (25-го и 75-го процентилей). Различия средних значений считаются статистически достоверными, если уровень значимости не превышал 0,05.
Для выявления взаимосвязи между переменными использовали коэффициент парной корреляции Пирсона (r). Корреляционные зависимости были распределены по силе связи: сильная (r=1,0-0,8), умеренная (r=0,79-0,6) и слабая (r=0,4-0,6).
Результаты и обсуждение
Все наблюдаемые дети родились в результате осложненного течения беременности: угрозы прерывания, преэклампсии, хронической фетоплацентарной недостаточности (ХФПН), перенесенных ОРВИ в ранние сроки беременности, новой короновирусной инфекции (НКВИ), а более 84,6% детей родились в результате оперативных родов (кесарева сечения).
Основные антропометрические показатели у новорожденных основной группы были достоверно ниже показателей группы сравнения, самыми низкими у детей с массой от 500 до 750 г. Основные данные представлены на рисунке 1 и 2.
К концу неонатального периода у всех детей, рожденных в сроке СПР, сформировалось перинатальное поражение центральной нервной системы различной степени тяжести.
Структура неврологической патологии у наблюдаемых детей представлена в таблице 1.
Церебральная ишемия 3-й степени определялась у 26,7% детей 1 подгруппы (500-750 г.), у 41,7% детей 2 подгруппы (от 751 г. и более) и не обнаружено у детей группы сравнения, (р1-3=0,003; р2-3=0,004; р1-2=0,002). Церебральная ишемия 2-й степени встречалась у детей: в 1 подгруппе — в 73,3%, во 2 подгруппе — в 55,6% и в группе сравнении — в 48,1% (р1-3=0,003; р2-3=0,004; р1-2=0,002), соответственно. Церебральная ишемия 1-й степени встречалась 2,6% у одного ребенка во 2 подгруппе. Ишемически-геморрагическое поражение ЦНС — церебральная ишемия в сочетании с внутрижелудочковым кровоизлиянием I–III степени (по классификации ВОЗ) — диагностировалось у детей со сроком гестации 23-27,6 недель чаще, чем у недоношенных с большим гестационным сроком (80% случаев в 1 подгруппе, 50% случаев во 2 подгруппе и 10,7% в группе сравнения). Следует отметить, что ВЖК II-III степени встречались у детей с гестационным возрастом 23-27,6 недель и у 1 ребенка группы сравнения, рожденного в сроке гестации 32 недели. У 1 ребенка 2-й группы на фоне ВЖК III степени сформировалась окклюзионная гидроцефалия, потребовавшая оперативного вмешательства. Данные отражены в таблице 2 и 3.
Таким образом, патология ЦНС у детей, рожденных в сроке СПР, встречалась достоверно чаще и была более выраженной, по сравнению с детьми группы сравнения. Наиболее выраженные изменения диагностированы у детей 1 подгруппы (500–750 г.). Наши данные согласуются с результатами других исследователей [4][13].
Контрольными точками нашего исследования был возраст детей 6 и 12 месяцев. Показатели физического развития детей в этом возрасте представлены на рисунке 3 и 4.
У детей, родившихся в сроке СПР, наблюдалось достоверное отставание в физическом развитии в течение 1 года жизни, более выраженнее у детей с массой при рождении 500-750 г. Дети группы сравнение имели среднее и высокое физическое развитие, и в 90,9 % гармоничный морфофункциональный статус.
Структура неврологических синдромов у детей на протяжении первого года жизни, родившихся в сроке СПР, представлена в таблицах 2 и 3.
В возрасте 6 месяцев у наблюдаемых детей, преобладал синдром двигательных нарушений в форме пирамидной недостаточности (53,3% случаев в 1 подгруппе, 44,4% случаев во 2 подгруппе и 25% в группе сравнения (р1-3=0,005; р2-3=0,002; р1-2=0,002). Достоверно чаще у глубоко недоношенных детей встречался синдром вегетативных дисфункций и также наиболее высокие показатели были у детей из первой подгруппы — 73,3%, во второй подгруппе — 50%, в группе сравнения — 17,9% (р1-3=0,002; р2-3=0,005; р1-2=0,004). Гипертензионно-гидроцефальный синдром достоверно чаще встречался в группе недоношенных детей с одинаковой частотой в основных подгруппах: 53,3% и 66,7% соответственно (р1-p2 = 0,005).
Синдром повышенной нервно-рефлекторной возбудимости (СПНРВ) имел место в основном у детей из 1 подгруппы — в 26,7%, во второй подгруппе — 13,9% и в группе сравнения в 10.7% случаев (р1-3=0,003; р2-3=0,004; р1-2=0,002)
Миатонический синдром с одинаковой частотой встречался у детей из основной группы (р1-p2 = 0,004).
К 12 месяцам жизни практически у всех детей основной группы сохранялись клинические проявления перинатального поражения центральной нервной системы, у детей основной группы 97,2% случаев и 48,1% группы сравнения.
Наблюдался синдром двигательных нарушений преимущественно в виде пирамидной недостаточности в 60% случаев в 1 подгруппе, 69,4% во 2 подгруппе и 10,7% в группе сравнения (р1-3=0,002; р2-3=0,002; р1-2=0,004). Практически в 2 раза уменьшились проявления гипертензионно гидроцефального синдрома среди недоношенных детей основной группы. Оставалась высокой частота встречаемости синдрома вегетативных дисфункций среди детей основной группы: 66,7 % и 44,4 % (Р1-2 = 0,003). К 12 месяцам жизни выросла частота миатонического синдрома и встречался он в большей степени у детей первой подгруппы 53,3% (Р1-2 = 0,003).
Инвалидность среди наблюдаемых нами глубоконедоношенных детей была оформлена у 4 детей (26,7%) — 1 подгруппы и 1 ребенка (2,8%) — 2 подгруппы, в виде детского церебрального паралича (ДЦП).
Основные клинические состояния сердечно-сосудистой системы у детей в возрасте 6 месяцев представлены на рисунках 5, 6, 7, 8.
К 12 месяцам жизни отчетливой положительной динамики в клинической картине не наблюдается. Клинические проявления нарушения функционального состояния сердечно-сосудистой системы в 12 месяцев характеризовались следующими признаками: среднее ЧСС составляло 127±11,4 уд. в мин. в 1 подгруппе, 124±15,2 уд. в мин во 2 подгруппе и 118±14 в группе сравнения (р1-p2=0,004; р1-3=0,001, р2-3=0,002), бледностью кожного покрова (1 подгруппа — 40%, 2 подгруппа — 27% и в группе сравнения — 3,7% (р1-p2=0,002; р1-3=0,005, р2-3=0,001), мраморностью (1 подгруппа — 60%, 2 подгруппа — 36,1% и в группе сравнения — 11,1% (р1-2=0,002; р1-3=0,002; р2-3=0,005); вегетососудистой лабильностью (1 подгруппа — 33,3%, 2 подгруппа — 19,4% (р1-2=0,001), соответственно; акроционозом (1 подгруппа — 40%, 2 подгруппа — 33,3% и в группе сравнения — 14,8% (р1-2=0,003; р1-3=0,002; р2-3=0,005); цианозом носогубного треугольника: (1 подгруппа — 13,3%, 2 подгруппа — 11,1% и в 3,7% случаев в группе сравнения (р1-2=0,002; р1-3=0,005; р2-3=0,001), соответственно), дистальным гипергидрозом: (1 подгруппа — 46,7%, 2 подгруппа — 27,8% и в группе сравнения 11,1% (р1-2=0,001; р1-3=0,003; р2-3=0,003); Похолоданием дистальных отделом конечностей: 1 подгруппа — 53,3%, 2 подгруппа — 30,5% и в группе сравнения 11,1% (р1-2=0,001; р1-3=0,003; р2-3=0,004). Нарушения сердечного ритма регистрировались у детей, рожденных от СПР: тахикардия (1 подгруппа — 20%, 2 подгруппа — 16% и в группе сравнения 7,4% (р1-2=0,002; р1-3=0,005; р2-3=0,001); брадикардия (1 подгруппа — 35,5%, 2 подгруппа — 16,1% и в группе сравнения 7,1% (р1-2=0,002; р1-3=0,005; р2-3=0,001); экстрасистолия (1 подгруппа — 13,3%, 2 подгруппа — 11,1% (р1-2=0,004), соответственно; аритмия (1 подгруппа — 13,3%, 2 подгруппа — 11,1% и в группе сравнения 7,1% (р1-2=0,002; р1-3=0,005; р2-3=0,001. Изменение характеристики сердечных тонов встречалось в виде: приглушенности (1 подгруппа — 26,7%, 2 подгруппа — 19,4% и в группе сравнения 11,1% (р1-2=0,002; р1-3=0,005; р2-3=0,001); систолического шума (1 подгруппа — 60%, 2 подгруппа — 44,4% и в группе сравнения 14,3% (р1-2=0,002; р1-3=0,005; р2-3=0,001); Грубый систолический шум встречался только в 1 подгруппе в 6,7% случаев.
Всем наблюдаемым детям проводилось электрокардиографическое исследование в динамике 6 и 12 месяцев (Таблица 4, 5). У наблюдаемых детей в возрасте 6 месяцев жизни нормальная ЭКГ зарегистрирована у 13,3% детей 1 подгруппы, у 16,7% — 2 подгруппы и 39,3% у детей группы сравнения соответственно (р1-2=0,003; р1-3=0,002; р2-3=0,004). В остальных случаях были выявлены нарушения сердечного ритма в виде синусовой аритмии, синусовой тахи- и брадикардии, экстрасистолии, предсердного ритма, миграции водителя ритма, суправентрикулярной пароксизмальной тахикардии, WPW синдрома, синдрома удлиненного интервала QT, что составило у детей 1 подгруппы 86,7% случаев, у детей 2 подгруппы 82,2% и 60,7% у детей группы сравнения (р1-2=0,003; р1-3=0,004; р2-3=0,004).
Нарушение проводимости в виде неполной блокады правой ножки пучка Гиса выявлено 66,7% в 1 подгруппе, 13,9% во 2 подгруппе и 3,6% в группе сравнения(р1-2=0,005; р1-3=0,003; р2-3=0,005). Атриовентрикулярная блокада 1 степени встречалась 26,7% в 1 подгруппе, 16,7% во 2 подгруппе и 7,1% в группе сравнения (р1-2=0,004; р1-3=0,002; р2-3=0,004).
Метаболические изменения в миокарде встречались 53,3% случаев в 1 подгруппе, 33% случаев во 2 подгруппе и 7,1% в группе сравнения (р1-2=0,002; р1-3=0,001; р2-3=0,005), соответственно.
К возрасту 12 месяцев у наблюдаемых детей показатели ЭКГ соответствовали норме 17,65%, у остальных детей основной группы выявлялись различные нарушения ритма в 82,35% случаев, метаболические изменения в миокарде были выявлены в 39,2% случаев в основной группе. В группе сравнения нормальное ЭКГ выявлялось в 64,3% случаев, нарушение сердечного ритма было обнаружено в 35,7% случаев. Метаболические изменения в миокарде выявлялись 7,1%.
Удлинение интервала QT обнаружено в 1 подгруппе в 33,3%, в 25% во 2 подгруппе (р1-2=0,001), соответственно. Интервал QТ — один из наиболее значимых параметров ЭКГ. Удлинение интервала QТ любого генеза является независимым фактором риска развития желудочковых тахиаритмий и внезапной сердечной смерти. QТc (корригированный) — величина, не зависящая от уровня ЧСС. Типы нарушения ритма сердца имеют прогностическое значение и определяют клиническое течение аритмии от бессимптомного, до выраженных субъективных жалоб, резко ухудшающих качество жизни и способствуют развитию жизнеугрожающих состояний. Кроме того, из обследованных детей основной группы, было 4 ребенка из 1 подгруппы, 3 детей из 2 подгруппы, у которых было сочетание нескольких типов нарушения ритма и проводимости сердца. Высокая распространенность (40–60%) малосимптомного и бессимптомного течения аритмии у детей различных возрастов определяет частый случайный характер обнаружения нарушений ритма сердца. У детей первого года жизни отмечается положительная динамика в виде снижения частоты встречаемости синдрома удлиненного интервала QT.
Установлена прямая сильная корреляционная связь между клиническими проявлениями вегетативных дисфункций в возрасте 6 месяцев и частотой выявленных дисфункций на ЭКГ (r=0,001) (p=0,001).
Установлена прямая сильная корреляционная связь между клиническими проявлениями вегетативных дисфункций в возрасте 12 месяцев и частотой выявленных дисфункций на ЭКГ (r=0,001) (p=0,001).
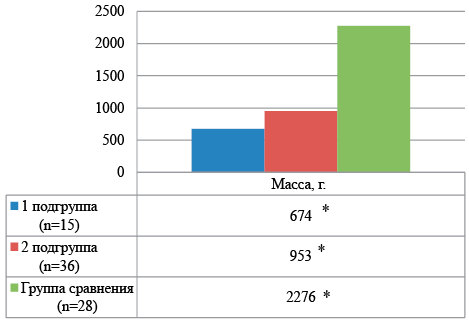
Примечание: *р1-2 — достоверность различий между 1 и 2 группами, р1-3 — достоверность различий между 1 и 3 группами, р2-3 — достоверность различий между 2 и 3 группами
Рисунок 1. Средние показатели массы тела (г) наблюдаемых детей при рождении
Figure 1. Average body weight (g) of observed children at birth
Таблица 1. Структура неврологической патологии у наблюдаемых детей, рожденных в сроке сверхранних преждевременных родов, при рождении (абс, %)
Table 1. Structure of neurological pathology in observed children born at very early preterm birth, at birth (abs, %)
Показатели | 1 подгруппа (n=15) | 2 подгруппа (n=36) | Группа сравнения (n=28) | Достоверность различий P | |||
Абс | % | Абс | % | Абс | % | ||
Гипоскически-ишемическая энцефалопатия: Церебральная ишемия 2 ст, Церебральная ишемия 3 ст, | 11 4 | 73,3 26,7 | 20 15 | 55,6 41,7 | 13 - | 48,1 - | P1 = 0,003 P2 = 0,004 P3 = 0,002 |
Ишемически-геморрагическое поражение ЦНС | 12 | 80,0 | 18 | 50 | 3 | 10,7 | P1 = 0,002 P2 = 0,003 P3 = 0,005 |
ВЖК I ст. | 4 | 26,7 | 7 | 19,4 | 2 | 7,1 | P1 = 0,005 |
ВЖК II ст. | 5 | 33,3 | 8 | 22,2 | 1 | 3,6 | P1 = 0,004 |
ВЖК III ст. | 3 | 20 | 3 | 8,3 | - | - | P1 = 0,003 |
Примечание: P1 — достоверность различий между показателями 1 подгруппы и 2 подгруппы; P2 — достоверность различий между показателями 1 подгруппы и группы сравнения; P3 — достоверность различий между показателями 2 подгруппы и группы сравнения
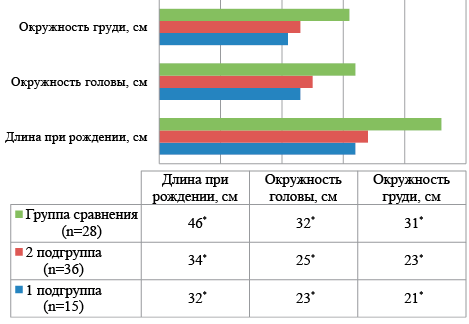
Примечание: *р1-2 — достоверность различий между 1 и 2 группами, р1-3 — достоверность различий между 1 и 3 группами, р2-3 — достоверность различий между 2 и 3 группами
Рисунок 2. Средние показатели длины тела (см) наблюдаемых детей при рождении
Figure 2. Average body length (cm) of observed children at birth
Таблица 2. Структура неврологических синдромов у детей, рожденных в сроке сверхранних преждевременных родов, в возрасте 6 месяцев жизни (абс, %)
Table 2. Structure of neurological syndromes in children born during very early preterm birth, at the age of 6 months of life (abs, %)
Показатели | 1 подгруппа (n=15) | 2 подгруппа (n=36) | Группа сравнения (n=28) | Достоверность различий p | |||
Абс | % | Абс | % | Абс | % | ||
Синдром вегето-сосудистых дисфункции | 11 | 73,3 | 18 | 50 | 5 | 17,9 | P p1-p2 = 0,002 P p1-p3 = 0,005 P p2-p3 = 0,004 |
Миатонический синдром | 4 | 26,7 | 10 | 27,8 | 2 | 7,1 | P p1-p2 = 0,004 P p1-p3 = 0,002 P p2-p3 = 0,001 |
Синдром пирамидной недостаточности | 8 | 53,3 | 16 | 44,4 | 7 | 25 | P p1-p2 = 0,005 P p1-p3 = 0,002 P p2-p3 = 0,002 |
Повышенная нервно-рефлекторная возбудимость | 4 | 26,7 | 5 | 13,9 | 3 | 10,7 | P p1-p2 = 0,003 P p1-p3 = 0,004 P p2-p3 = 0,002 |
Окклюзионная гидроцефалия | - | - | 1 | 2,8 | - | - | P p1-p2 = NS |
Синдром дефицита внимания | 2 | 13,3 | 4 | 11,1 | - | - | P p1-p2 = 0,002 |
Гипертензионно-гидроцефальный синдром (ГГС) | 8 | 53,3 | 24 | 66,7 | 5 | 17,9 | P p1-p2 = 0,005 P p1-p3 = 0,004 P p2-p3 = 0,004 |
Примечание: NS — not significant (англ.) — не значимо, р1-2 — достоверность различий между 1 и 2 группами, р1-3 — достоверность различий между 1 и 3 группами, р2-3 — достоверность различий между 2 и 3 группами
Таблица 3. Структура неврологических синдромов у детей, рожденных в сроке сверхранних преждевременных родов, в возрасте 12 месяцев жизни (абс, %)
Table 3. Structure of neurological syndromes in children born during very early preterm birth, at the age of 12 months of life (abs, %)
Показатели | 1 подгруппа (n=15) | 2 подгруппа (n=36) | Группа сравнения (n=28) | Достоверность различий p | |||
Абс | % | Абс | % | Абс | % | ||
Синдром вегето-сосудистых дисфункции | 11 | 73,3 | 18 | 50 | 5 | 17,9 | P p1-p2 = 0,002 P p1-p3 = 0,005 P p2-p3 = 0,004 |
Миатонический синдром | 8 | 53,3 | 15 | 41,7 | 3 | 10,7 | P p1-p2 = 0,003 P p1-p3 = 0,005 P p2-p3 = 0,002 |
Синдром пирамидной недостаточности | 9 | 60 | 25 | 69,4 | 3 | 10,7 | P p1-p2 = 0,002 P p1-p3 = 0,002 P p2-p3 = 0,004 |
Синдром повышенной нервно-рефлекторной возбудимости (СПНРВ) | 2 | 13,3 | 3 | 8,3 | 1 | 3,6 | P p1-p2 = 0,005 P p1-p3 = 0,003 P p2-p3 = 0,004 |
Окклюзионная гидроцефалия | - | - | 1 | 2,8 | - | - | P p1-p2 = NS |
Синдром дефицита внимания | 2 | 13,3 | 1 | 2,8 | - | - | P p1-p2 = 0,005 |
Гипертензионно-гидроцефальный синдром (ГГС) | 5 | 33,3 | 11 | 30,6 | 2 | 7,1 | P p1-p2 = 0,005 P p1-p3 = 0,002 P p2-p3 = 0,001 |
Детский церебральный паралич (ДЦП) | 4 | 26,7 | 1 | 2,8 | - | - | P p1-p2 = 0,003 |
Примечание: NS — not significant (англ.) — не значимо, р1-2 — достоверность различий между 1 и 2 группами, р1-3 — достоверность различий между 1 и 3 группами, р2-3 — достоверность различий между 2 и 3 группами
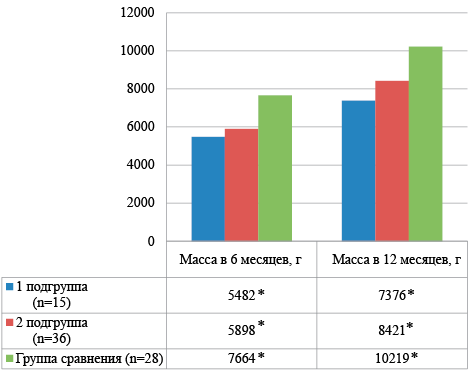
Примечание:*р1-2 — достоверность различий между 1 и 2 группами, р1-3 — достоверность различий между 1 и 3 группами, р2-3 — достоверность различий между 2 и 3 группами
Рисунок 3. Средние показатели массы тела (г) у обследованных детей в возрасте 6 и 12 месяцев
Figure 3. Average body weight (g) in examined children aged 6 and 12 months
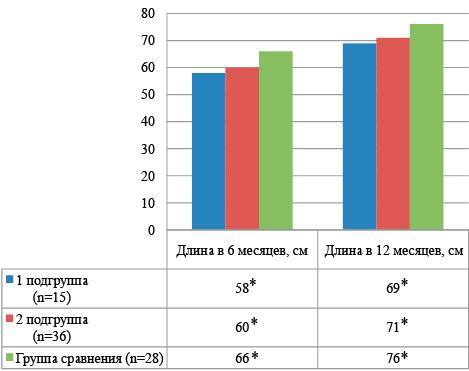
Примечание:*р1-2 — достоверность различий между 1 и 2 группами, р1-3 — достоверность различий между 1 и 3 группами, р2-3 — достоверность различий между 2 и 3 группами
Рисунок 4. Средние показатели длины тела (см) у обследованных детей в возрасте 6 и 12 месяцев
Figure 4. Average body length (cm) in examined children aged 6 and 12 months
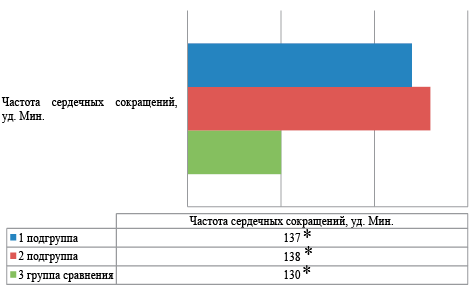
Примечание: *р1-2 — достоверность различий между 1 и 2 группами, р1-3 — достоверность различий между 1 и 3 группами, р2-3 — достоверность различий между 2 и 3 группами
Рисунок 5. Средняя частота сердечных сокращений (уд. мин) у обследованных детей в возрасте 6 месяцев
Figure 5. Average heart rate (bpm) in examined children aged 6 months
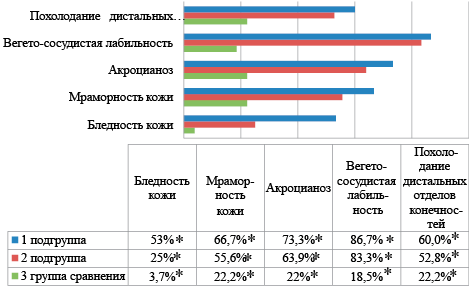
Примечание:*р1-2 — достоверность различий между 1 и 2 группами, р1-3 — достоверность различий между 1 и 3 группами, р2-3 — достоверность различий между 2 и 3 группами
Рисунок 6. Клинические проявления вегетативных дисфункций (%) у обследованных детей в возрасте 6 месяцев
Figure 6. Clinical manifestations of autonomic dysfunctions (%) in examined children aged 6 months
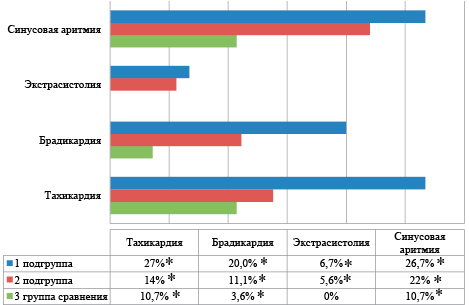
Примечание:*р1-2 — достоверность различий между 1 и 2 группами, р1-3 — достоверность различий между 1 и 3 группами, р2-3 — достоверность различий между 2 и 3 группами
Рисунок 7. Клинические проявления нарушений сердечного ритма (%) у обследованных детей в возрасте 6 месяцев
Figure 7. Clinical manifestations of heart rhythm disturbances (%) in examined children aged 6 months
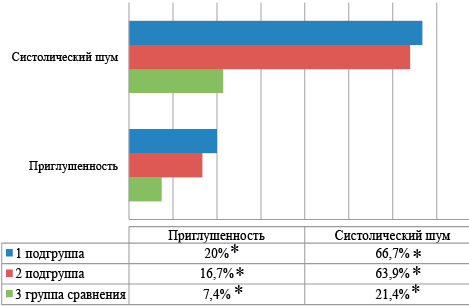
Примечание: *р1-2 — достоверность различий между 1 и 2 группами, р1-3 — достоверность различий между 1 и 3 группами, р2-3 — достоверность различий между 2 и 3 группами
Рисунок 8. Оценка характеристики сердечных тонов (%) у обследованных детей в возрасте 6 месяцев
Figure 8. Assessment of the characteristics of heart sounds (%) in examined children at the age of 6 months
Таблица 4. Результаты ЭКГ у детей в возрасте 6 месяцев, родившихся в сроке сверхранних преждевременных родов (абс., %)
Table 4. ECG results in children aged 6 months born in very early preterm labor (abs., %)
Наименование признака | 1 подгруппа (n=15) | 2 подгруппа (n=36) | 3 группа сравнения (n=28) | Достоверность различий; p | |||
Абс | % | Абс | % | Абс | % | ||
Нормальная ЭКГ | 2 | 13,3 ±0,35 | 6 | 16,7±0,45 | 11 | 39,3±0,49 | P1 = 0,003 P2 = 0,002 P3=0,004 |
Нарушение сердечного ритма и проводимости: - синусовая тахикардия | 5 | 33,3±0,49 | 15 | 41,7±0,50 | 2 | 7,1±0,22 | P1 = 0,003 P2= 0,002 P3=0,001 |
- синусовая брадикардия | 4 | 26,7±0,46 | 6 | 16,7±0,38 | 4 | 14,3±0,36 | P1 = 0,003 P2= 0,005 P3=0,004 |
- эктрасистолия | 2 | 13,3±0,35 | 2 | 5,7±0,23 | - | - | P1 = 0,003 |
-синусовая аритмия | 4 | 26,7±0,46 | 8 | 22,2±0,42 | 6 | 10,7±0,42 | P1 = 0,002 P2= 0,005 P3=0,005 |
- предсердный ритм | 3 | 20±0,41 | 2 | 5,6±0,23 | 1 | 3,6±0,19 | P1 = 0,002 P2= 0,004 P3=0,005 |
- миграция водителя ритма | 3 | 13,3±0,35 | 2 | 5,6±0,23 | - | - | P1 = 0,004 P2= 0,005 P3=0,005 |
- Пароксизмальная тахикардия | 4 | 26,7±0,46 | 2 | 5,6±0,23 | - | - | P1 = 0,003 P2= 0,005 P3=0,004 |
Атриовентрикулярная блокада 1 степени | 4 | 26,7±0,46 | 6 | 16,7±0,38 | 2 | 7,4±0,27 | P1 = 0,004 P2= 0,005 P3=0,004 |
-WPW синдром | 3 | 20±0,41 | 5 | 13,9±0,35 | - | 3,6±0,19 | P1 = 0,004 P2= 0,005 P3=0,004 |
Синдром удлиненного QT | 10 | 66,8±0,49 | 17 | 47,2±0,51 | 1 | 7,1±0,27 | P1 = 0,005 P2= 0,003 P3=0,004 |
Метаболические нарушения в миокарде | 8 | 53,3±0,52 | 12 | 33,3±0,4 | 2 | 7,1±0,27 | P1 = 0,003 P2= 0,005 P3=0,004 |
Примечание: P1 — достоверность различий между показателями 1 подгруппы и 2 подгруппы, P2 — достоверность различий между показателями 1 подгруппы и группы сравнения, P3 — достоверность различий между показателями 2 подгруппы и группы сравнения
Таблица 5. Результаты ЭКГ у детей в возрасте 12 месяцев, родившихся в сроке сверхранних преждевременных родов (абс., %)
Table 5. ECG results in children aged 12 months born in very early preterm birth (abs., %)
Наименование признака | 1 подгруппа (n=15) | 2 подгруппа (n=36) | 3 группа сравнения (n=28) | Достоверность различий p | |||
Абс | % | Абс | % | Абс | % | ||
Нормальная ЭКГ | 1 | 6,7±0,20 | 8 | 22,2±0,42 | 8 | 64,3±0,51 | P1 = 0,003 P2= 0,005 P3=0,001 |
Нарушение сердечного ритма и проводимости: -синусовая тахикардия | 6 | 40±0,51 | 7 | 19,4±0,4 | 4 | 14,3±0,36 | P1 = 0,005 P2= 0,002 P3=0,004 |
-синусовая брадикардия | 6 | 40±0,49 | 4 | 11,1±0,32 | 3 | 10,7±0,32 | P1 = 0,003 P2= 0,003 P3=0,004 |
- эктрасистолия | 4 | 26,7±0,35 | 3 | 7,1±0,23 | - | - | P1 = 0,003 |
-синусовая аритмия | 5 | 33,3±0,49 | 6 | 16,7±0,38 | 3 | 10,7±0,27 | P1 = 0,003 P2= 0,003 P3=0,004 |
- предсердный ритм | 5 | 33,3±0,46 | 4 | 11,1±0,32 | - | - | P1 = 0,005 |
- миграция водителя ритма | 5 | 33,3±0,41 | 4 | 11,1±0,32 | 3 | 10,7±0,32 | P1 = 0,005 P2= 0,002 P3=0,004 |
- Пароксизмальная тахикардия | 4 | 26,7±0,47 | 3 | 7,1±0,27 | - | - | P1 = 0,005 |
Атриовентрикулярная блокада 1 степени | 3 | 20±0,41 | 4 | 11,1±0,32 | 1 | 3,6±0,19 | P1 = 0,003 P2= 0,005 P3=0,004 |
WPW синдром | 1 | 6,7±0,26 | 4 | 11,1±0,32 | - | - | P1 = 0,003 |
Синдром удлиненного QT | 5 | 33,3±0,49 | 9 | 25±0,44 | - | - | P1 = 0,003 |
Метаболические нарушения в миокарде | 2 | 13,3±0,35 | 10 | 27,8±0,45 | 2 | 7,1±0,27 | P1 = 0,003 P2= 0,005 P3=0,004 |
Примечание: P1 — достоверность различий между показателями 1 подгруппы и 2 подгруппы, P2 — достоверность различий между показателями 1 подгруппы и группы сравнения, P3 — достоверность различий между показателями 2 подгруппы и группы сравнения
Заключение
У детей, рожденных в сроке СПР, на первом году жизни регистрируются разнообразные ЭКГ-феномены. С наибольшей частотой выявляются нарушения сердечного ритма и проводимости в виде синусовой тахи- и брадикардии, экстрасистолии, синусовой аритмии, эктопического ритма, суправентрикулярной параксизмальной тахикардии, антриовентрикулярной блокады, неполной блокады правой ножки пучка Гиса, синдрома WPW. У части детей был обнаружен синдром удлиненного интервала QT.
В динамике первого года жизни отчетливой положительной тендеции не наблюдается. В наиболее неблагоприятной ситуации находятся дети, рожденные с массой от 500 до 750 г.
Полученные результаты обусловлены крайней незрелостью при рождении, в том числе проводящей системы сердца, а также наличием перинатального поражения ЦНС различной степени тяжести, влекущей за собой нарушение центральной регуляции сердечного ритма.
Вегетативная регуляция сердечного ритма у детей на сегодняшний день остается актуальной проблемой не только педиатров, но и для узких специалистов в целом. Это связано с тем, что в постнатальном периоде происходит интенсивный процесс балансировки симпатических и парасимпатических влияний, определяющих иннервацию сердца. Нарушения этого баланса может потенциально повлиять на реализацию риска аритмии, в последующим может привести к патологии в сердце и в организме в целом. Симпатическая гиперактивация свидетельствует о высокой степени электрической нестабильности миокарда. Сохраняющиеся изменения вегетативной регуляции сердечного ритма, а именно гиперсимпатикотония, у глубоконедоношенных детей с перинатальным поражением ЦНС диктуют необходимость в дальнейшем диспансерном наблюдении неврологом и детским кардиологом.
Список литературы
1. Всемирная организация здравоохранения. Информационный бюллетень «Преждевременные роды» 23 Мая 2023 год. URL: https://www.who.int/ru/news-room/fact-sheets/detail/preterm-birth
2. Ковтун О.П., Цывьян П.Б., Маркова Т.В., Чумарная Т.В. Ремоделирование сердца недоношенных детей. Вестник РАМН. 2020;75(6):631-637. doi: https://doi.org/10.15690/vramn1268
3. Герасимова Л.И., Бушуева Э.В., Пигаваева А.Н., Ефимова О.С., Бушуев В.И., Иванова Э.А. Электрокардиографические и эхокардиографические особенности у детей до одного года с учетом массы тела при рождении. Современные проблемы науки и образования, 2013, (4), 103-103. https://elibrary.ru/download/elibrary_20848183_48631722.pdf
4. Соловьева, Г. А. Характеристика сердечного ритма у детей с перинатальным поражением центральной нервной системы (по данным катамнеза). Современная медицина: актуальные вопросы. 2013; 24: 27-31. https://elibrary.ru/download/elibrary_20380949_43457162.pdf
5. Безкаравайный, Б. А., Соловьева, Г. А., Репина, Г. И., Максименко, Ю. В. Особенности сердечного ритма у недоношенных новорожденных с перинатальным поражением центральной нервной системы. Здоровье ребенка. 2010;3:116-119. http://pediatric.mifua.com/archive/article/13002
6. Щербакова В.П. Состояние здоровья детей, рожденных с массой тела менее 1000 г, к возрасту трех лет. Российский педиатрический журнал. 2022;3(1):358, https://www.rospedj.ru/jour/issue/view/12/showToc
7. Leneuve-Dorilas M., Favre A., Louis A., Bernard S., Carles G., & Nacher M. Risk Factors for very preterm births in French Guiana: The burden of induced preterm birth. AJP reports. 2019;9(1):e44. https://doi.org/10.1055/s-0039-1678716
8. Мурсалова З. Ш. Г. Предикторы бронхолегочной дисплазии у детей грудного возраста, родившихся с низкой массой тела. European journal of biomedical and life sciences. 2020;4: 9-14. https://doi.org/10.29013/ELBLS-20-4-9-14
9. Радзинский В.Е., Оразмурадов А.А., Савенкоа И.В., Дамирова К.Ф., Хаддад Х. Преждевременные роды — нерешенная проблема XXI века. Кубанский научный медицинский вестник. 2020;27(4):27-37. https://doi.org/10.25207/1608-6228-2020-27-4-27-37
10. Долгова З.Р. Особенности перинатального анамнеза и вариабельности сердечного ритма у недоношенных детей первого года жизни, рожденных с экстремально низкой массой тела и очень низкой массой тела. Вестник современной клинической медицины. 2014; 7(6): 20-26. https://elibrary.ru/download/elibrary_22589600_10517403.pdf
11. Диаграммы INTERGROWTH-21st (Международный консорциум по росту плода и новорожденного). https://intergrowth21.tghn.org/interpractice-21st/interpractice-21st-study-documents/
12. Черная Н.Л., Маскова Г.С., Ганузин В.М., Шубина Е.В., Дадаева О.Б. Нормативы оценки антропометрических показателей у детей от 0 до 19 лет в соответствии с рекомендациями Всемирной организации здравоохранения — Ярославль, 2018. — 116 с.
13. Милованова ОА, Амирханова ДЮ, Миронова АК, Джуккаева ММ, Комиссарова ОА, Авакян ГГ. Риски формирования неврологической патологии у глубоконедоношенных детей: обзор литературы и клинические случаи. Медицинский Совет. 2021;1:20-29. https://doi.org/10.21518/2079-701X-2021-1-20-29
Об авторах
С. Ю. ЗахароваРоссия
Захарова Светлана Юрьевна — доктор медицинских наук, профессор, ведущий научный сотрудник.
ул. Репина, д. 1, Екатеринбург, 620028
О. С. Покусаева
Россия
Покусаева Оксана Сергеевна — аспирант Федерального государственного бюджетного учреждения «Уральский НИИ ОММ» МЗ РФ; врач детский–кардиолог ГАУЗ СО «Детская городская поликлиника №13» г. Екатеринбурга.
ул. Репина, д. 1, Екатеринбург, 620028; ул. Ткачей, д. 16а, Екатеринбург, 620100
Рецензия
Для цитирования:
Захарова С.Ю., Покусаева О.С. Результаты электрокардиографии у детей, родившихся в сроке сверхранних преждевременных родов. Вестник охраны материнства и младенчества. 2024;1(1):117-129. https://doi.org/10.69964/BMCC-2024-1-1-117-129
For citation:
Zakharova S.Yu., Pokusaeva O.S. Results of electrocardiography in children born at very early preterm birth. Bulletin of maternal and child care. 2024;1(1):117-129. (In Russ.) https://doi.org/10.69964/BMCC-2024-1-1-117-129









