Перейти к:
Влияние раствора хлоргексидина биглюконата на сохранность бактериальной ДНК и эффективность ПЦР
https://doi.org/10.69964/BMCC-2025-2-1-79-85
Аннотация
Введение. 0,05% раствор хлоргексидина биглюконата (ХБ) является одним из самых часто используемых антисептиков, при этом непонятно оказывает ли ХБ ингибирующее влияние на амплификацию нуклеиновых кислот в ходе полимеразной цепной ре акции (ПЦР). Цель исследования. Оценить влияние раствора хлоргексидина биглюконата на сохранность бактериальной ДНК и эффективность ПЦР. Материалы и методы. Исследована чувствительность смеси из культур Lactobacilllus acidophilus, Staphylococcus aureus и Escherichia coli к 0,05% раствору ХБ при 1, 2 и 7-днев ной экспозиции в условиях холодильника и морозильной камеры. Результаты. Раствор ХБ не приводил к ингибированию ПЦР и разрушению бактериальной ДНК ни одной из тестируемых групп бактерий через 1, 2 и 7 дней экспозиции как в условиях холодильника, так и в условиях морозильной камеры. Заключение. Полученные результаты позволяют в штатном режиме интерпретировать ПЦР-исследования на бактериальные инфекции и состав микробиоты даже в случае предварительной обработки слизистой 0,05% раствором хлоргексидина биглюконата.
Для цитирования:
Зорников Д.Л., Нечаева Д.М., Симарзина В.М., Корнилов Д.О., Карякина А.Е., Аминева П.Г., Ворошилина Е.С. Влияние раствора хлоргексидина биглюконата на сохранность бактериальной ДНК и эффективность ПЦР. Вестник охраны материнства и младенчества. 2025;2(1):79-85. https://doi.org/10.69964/BMCC-2025-2-1-79-85
For citation:
Zornikov D.L., Nechaeva D.M., Simarzina V.M., Kornilov D.O., Kariakina A.E., Amineva P.G., Voroshilina E.S. Impact of Chlorhexidine Digluconate on Bacterial DNA Preservation and PCR Efficiency. Bulletin of maternal and child care. 2025;2(1):79-85. (In Russ.) https://doi.org/10.69964/BMCC-2025-2-1-79-85
Введение
Хлоргексидина биглюконат (ХБ) является одним из самых используемых антисептиков. ХБ обладает доказанной активностью в отношении грамположительных и грамотрицательных бактерий [1]. Механизм действия заключается в разрушении клеточной стенки, что приводит к осмотическому шоку и гибели микроорганизмов [2]. Как правило, для обработки кожи и слизистых оболочек используются 0,05% раствор ХБ.
При этом в части инструкций к наборам реагентов для полимеразной цепной реакции (ПЦР) ХБ упоминается как интерферирующее вещество, способное оказывать воздействие на результаты ПЦР [3]. ХБ ингибирует РНК-зависимую РНК-полимеразу, связываясь с активным центром фермента [4], что не исключеет вероятности ингибирования других ферментов синтеза нуклеиновых кислот, включая Taq-полимеразу. Кроме того, было отмечено, что ХБ разрушает ДНК лейкоцитов [5], что заставляет рассматривать гипотетическую возможность разрушения микробной ДНК под воздействием ХГ. По этой причине у врачей часто возникает вопрос относительно достоверности результатов ПЦР-исследования, если пациент перед сдачей биоматериала обрабатывал слизистую ХБ, в том числе слизистую носоглотки при сдаче на респираторные инфекции и слизистую урогенитального тракта при исследовании на микробиоту и инфекции, передаваемые половым путем.
Цель исследования — оценить влияние раствора хлоргексидина биглюконата на сохранность бактериальной ДНК и эффективность ПЦР.
Материалы и методы
Для оценки влияния ХБ на сохранность бактериальной ДНК и эффективность ПЦР готовили 7 серий пробирок: по 3 пробирки с 900 мкл 0,05% ХБ и 1 контрольной пробирке с 900 мкл физиологического раствора (всего 28 пробирок — 21 с ХБ и 7 контрольных). Во все пробирки вносили по 100 мкл. смеси бактериальных культур Lactobacillus acidophilus, Staphylococcus aureus и Escherichia coli (плотность каждой культуры 0,5 по Макфарленду) (Рисунок 1).
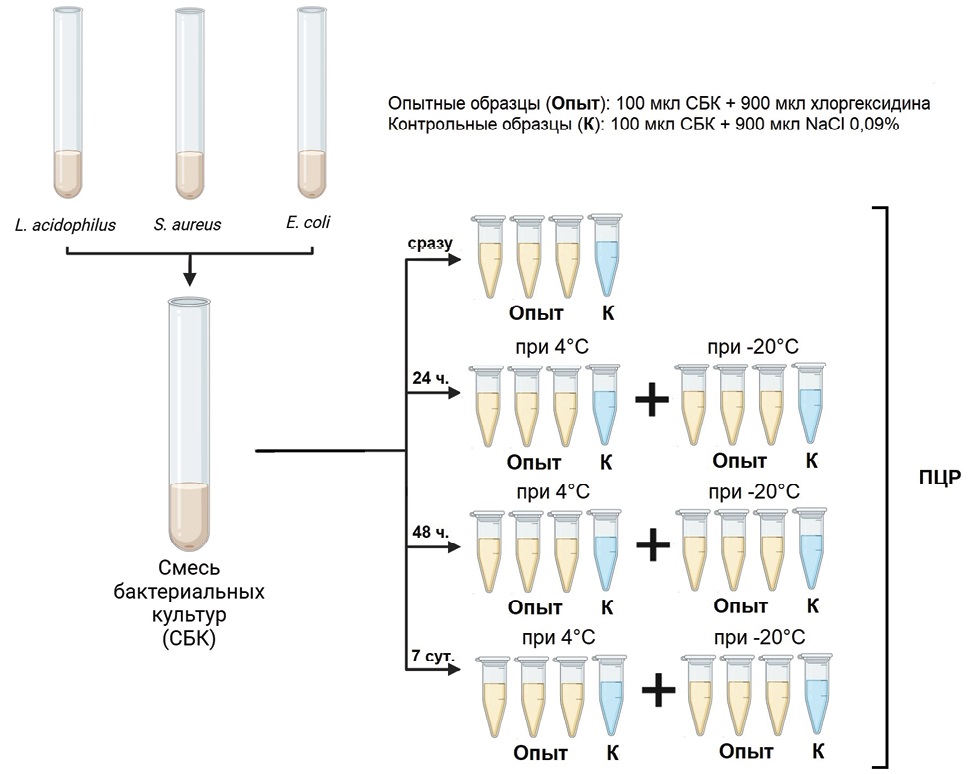
Рисунок 1. Дизайн исследования влияния раствора хлоргексидина биглюконата на сохранность бактериальной ДНК и эффективность ПЦР
Figure 1. Design of a study of the impact of chlorhexidine digluconate solution on bacterial DNA preservation and PCR efficiency
Из первой серии пробирок провели выделение ДНК сразу после приготовления суспензий, 3 серии пробирок поместили в холодильник (+4 °C) и 3 — в морозильную камеру (-20 °C). Через 1, 2 и 7 суток хранения изымали по одной серии пробирок из холодильника и морозильной камеры и проводили выделение ДНК.
Выделение ДНК осуществляли набором Проба-НК-ПЛЮС (ООО ДНК-Технология, Россия). Выделенную ДНК исследовали набором для ПЦР-диагностики “Андрофлор” (ООО ДНК-Технология, Россия). Полученные результаты по Lactobacillus spp, Staphylococcus spp и группе Enterobacteriaceae/Enterococcus (группа EE) сравнивали в экспериментальных и контрольных образцах, рассчитывая отклонение каждого показателя в экспериментальных образцах от аналогичного показателя в контрольном образце серии по следующей формуле:
Δ = 2CpБХ – CpХ,
где Δ — отклонение показателя в эксперименте с ХБ от показателя в контроле, показывает во сколько раз количество целевой группы отличается в эксперименте от контроля при максимальной эффективности ПЦР; CpБХ — индикаторный цикл амплификации для целевой группы бактерий в контрольном образце без ХБ; CpХ — индикаторный цикл амплификации для целевой группы бактерий в экспериментальном образце с ХБ.
Результат представляли как медиану по 3 экспериментальным пробиркам серии со значениями 1-го и 3-го квартилей.
Статистическую обработку и визуализацию данных проводили с помощью R версии 4.4.3. В качестве меры центральной тенденции при описании переменных указывали медиану со значениями 1-го и 3-го квартилей.
Результаты
В случае выделения ДНК непосредственно после приготовления образцов получали сопоставимые результаты в пробах с ХБ и без ХБ по показателям Lactobacillus spp и Staphylococcus spp, тогда как количества бактерий группы EE были на 0.3 (0.2; 0.4) lg выше в образцах с ХБ (Рисунок 2).
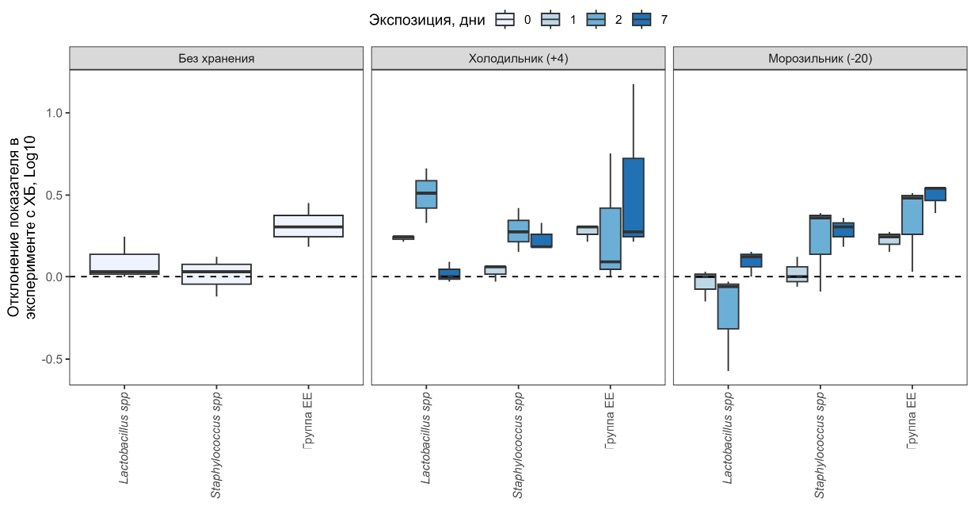
Рисунок 2. Влияние раствора хлоргексидина биглюконата на бактериальную ДНК и эффективность ПЦР in vitro
Figure 2. Impact of the chlorhexidine digluconate solution on bacterial DNA preservation and PCR efficiency in vitro
В образцах, хранившихся в холодильнике (+4 °C), вне зависимости от времени хранения и группы бактерий не отмечали ингибирующего эффекта ХБ на ПЦР. Изменение лактобацилл в экспериментальных образцах составили 0.2 (0.2; 0.2) lg — через сутки, 0.5 (0.4; 0.6) lg — через двое суток и 0 (0; 0) lg — через 7 суток. Количество стафилококков изменилось на 0.1 (0; 0.1) lg — через сутки, на 0.3 (0.2; 0.3) lg — через двое суток и на 0.2 (0.2; 0.3) lg — через 7 суток. Изменения количества группы EE составили 0.3 (0.3; 0.3) lg — через сутки, 0.1 (0; 0.4) lg — через двое суток и 0.3 (0.2; 0.7) lg — через 7 суток.
В хранившихся в морозильнике экспериментальных образцах (-20 °C) количество лактобацилл изменялось на 0 (-0.1; 0) lg — через сутки, на -0.1 (-0.3; 0) lg — через двое суток и на 0 (0; 0) lg — через 7 суток. Количество стафилококков изменилось на 0 (0; 0.1) lg — через сутки, на 0.4 (0.1; 0.4) lg — через двое суток и на 0.3 (0.2; 0.3) lg — через 7 суток. Изменения количества группы EE составили 0.2 (0.2; 0.3) lg — через сутки, 0.5 (0.3; 0.5) lg — через двое суток и 0.5 (0.5; 0.5) lg — через 7 суток.
Обсуждение
ХБ не оказывал ингибирующего влияния на результаты ПЦР при исследовании на грамположительные и грамотрицательные бактерии. Выделение ДНК преципитационным методом как сразу после приготовления бактериальных суспензий в ХБ, так и через 1-7 дней хранения не приводило к снижению эффективности ПЦР в опытных образцах. Результаты проведенного эксперимента позволяют предположить, что ХБ не оказывает влияния на Taq-полимеразу, либо используемые в протоколе выделения отмывки позволяют полностью избавиться от интерферирующей концентрации ХБ. По всей видимости, ХБ в концентрации 0,05% не оказывает разрушающего эффекта на бактериальную ДНК, так как концентрации целевой бактериальной ДНК при хранении в ХБ даже несколько превышали аналогичные концентрации для контрольных образцов без ХБ.
Заключение
7-суточная экспозиция Lactobacillus acidophilus, Staphylococcus aureus и Escherichia coli в 0,05% растворе хлоргексидина биглюконата, как при температуре +4 °C так и -20 °C, не приводила к снижению выхода ДНК и не ингибировала ПЦР в случае выделения ДНК преципитационным методом. Данное наблюдение позволяет интерпретировать результаты ПЦР-исследований на бактериальные инфекции и состав микробиоты даже в случае предварительной обработки слизистой 0,05% раствором хлоргексидина биглюконата.
ДЕКЛАРАЦИЯ О НАЛИЧИИ ДАННЫХ: данные, подтверждающие выводы настоящего исследования, можно получить у контактного автора по обоснованному запросу. Данные и статистические методы, представленные в статье, прошли статистическое рецензирование.
СООТВЕТСТВИЕ ПРИНЦИПАМ ЭТИКИ: проведенное исследование соответствует стандартам Хельсинкской декларации (Declaration Helsinki), одобрено Комитетом по этике Федерального государственного бюджетного образовательного учреждения высшего образования «Уральский государственный медицинский университет» Минздрава России (ул. Репина, д. 3, г. Екатеринбург, 620028, Россия) протокол № 4 от 26.05.2023.
ВКЛАД АВТОРОВ:
Е.С. Ворошилина, Д.Л. Зорников, П.Г. Аминева — разработка концепции и дизайна исследования; Д.М. Нечаева, В.М. Симарзина, Д.О. Корнилов, А.Е. Карякина — проведение исследования; Д.Л. Зорников, Д.М. Нечаева, В.М. Симарзина, А.Е. Карякина — анализ и интерпретация результатов, обзор литературы, статистическая обработка, составление черновика рукописи; Е.С. Ворошилина, Д.Л. Зорников, П.Г. Аминева — критический пересмотр черновика рукописи и формирование его окончательного варианта.
Все авторы одобрили финальную версию статьи перед публикацией, выразили согласие нести ответственность за все аспекты работы, подразумевающее надлежащее изучение и решение вопросов, связанных с точностью и добросовестностью любой части работы.
DATA AVAILABILITY STATEMENT: Data supporting the findings of this study are available from the corresponding author upon reasonable request. The data and statistical methods presented in the study have been statistically reviewed by the journal editor, a certified biostatistician.
COMPLIANCE WITH ETHICAL STANDARDS: The study complies with the standards of the Helsinki Declaration, approved by the Independent Committee for Ethics of Ural State Medical University of the Ministry of Health of Russian Federation (Repina St., 3, Ekaterinburg, 620028, Russia), protocol No. 4 from 26.05.2023.
AUTHOR CONTRIBUTIONS:
Ekaterina S. Voroshilina, Danila L. Zornikov, Polina G. Amineva — concept statement and contribution to the scientific layout, Diana M. Nechaeva, Veronika M. Simarzina, Daniil O. Kornilov, Anastasia E. Kariakina — conducting experiment; Danila L. Zornikov, Diana M. Nechaeva, Veronika M. Simarzina, Anastasia E. Kariakina — analysis and interpretation of the results, literature review, statistical analysis; Ekaterina S. Voroshilina, Danila L. Zornikov, Polina G. Amineva — drafting the manuscript and preparing; its final version; introduction of valuable intellectual content.
All authors approved the final version of the paper before publication and assume responsibility for all aspects of the work, which implies proper study and resolution of issues related to the accuracy and integrity of any part of the work.
Список литературы
1. Tavafi H, Sadrzadeh-Afshar M, Niroomand S. In vitro ef fectiveness of antimicrobial properties of propolis and chlorhexidine on oral pathogens: A comparative study: Effectiveness of antimicrobial properties of propolis and chlorhexidine on oral pathogens. Biosis: Biological Systems. 2020;1(3):116-125. https://doi.org/10.37819/biosis.001.03.0062
2. Kapralos V, et al. Effect of chlorhexidine digluconate on antimicrobial activity, cell viability and physicochemical properties of three endodontic sealers. dental materials. 2022;38(6):1044-1059. https://doi.org/10.1016/j.dental.2022.04.013
3. ДНК-Технология. (2023). Инструкция по применению набора реагентов для исследования микрофлоры урогенитального тракта мужчин методом ПЦР в режиме реального времени Андрофлор, Андрофлор Скрин, 393-5. [DNA Technology. (2023). Instructions for the use of a reagent kit for the examination of the microflora of the male urogenital tract by real-time PCR Androflor, Androflor Screen, 393-5. (In Russ.)]
4. Choudhury S, et al. Evaluating the potential of different inhibitors on RNA-dependent RNA polymerase of severe acute respiratory syndrome coronavirus 2: A molecular modeling approach. Medical Journal Armed Forces India. 2021;77:S373-S378. https://doi.org/10.1016/j.mjafi.2020.05.005
5. Ribeiro DA, et al. Chlorhexidine induces DNA damage in rat peripheral leukocytes and oral mucosal cells. Journal of periodontal research. 2004;39(5):358-361. https://doi.org/10.1111/j.1600-0765.2004.00759.x
Об авторах
Д. Л. ЗорниковРоссия
Зорников Данила Леонидович — кандидат медицинских наук, доцент, доцент кафедры медицинской микробиологии и клинической лабораторной диагностики
Адрес: ул. Репина, д. 3, г. Екатеринбург, 620028
Д. М. Нечаева
Россия
Нечаева Диана Мирзозоновна — лаборант кафедры медицинской микробиологии и клинической лабораторной диагностики
Адрес: ул. Репина, д. 3, г. Екатеринбург, 620028
В. М. Симарзина
Россия
Симарзина Вероника Михайловна — ассистент кафедры медицинской микробиологии и клинической лабораторной диагностики
Адрес: ул. Репина, д. 3, г. Екатеринбург, 620028
Д. О. Корнилов
Россия
Корнилов Даниил Олегович — ассистент кафедры медицинской микробиологии и клинической лабораторной диагностики
Адрес: ул. Репина, д. 3, г. Екатеринбург, 620028
А. Е. Карякина
Россия
Карякина Анастасия Евгеньевна — лаборант кафедры медицинской микробиологии и клинической лабораторной диагностики
Адрес: ул. Репина, д. 3, г. Екатеринбург, 620028
П. Г. Аминева
Россия
Аминева Полина Геннадьевна — ассистент кафедры медицинской микробиологии и клинической лабораторной диагностики; врач-бактериолог, заведующий лабораторией
Адрес: ул. Машинная, 1, г. Екатеринбург, 620028
Е. С. Ворошилина
Россия
Ворошилина Екатерина Сергеевна — доктор медицинских наук, профессор, заведующий кафедрой медицинской микробиологии и клинической лабораторной диагностики; заведующий лабораторным отделением
Адрес: ул. Тверитина, 16, Екатеринбург, 620028
Рецензия
Для цитирования:
Зорников Д.Л., Нечаева Д.М., Симарзина В.М., Корнилов Д.О., Карякина А.Е., Аминева П.Г., Ворошилина Е.С. Влияние раствора хлоргексидина биглюконата на сохранность бактериальной ДНК и эффективность ПЦР. Вестник охраны материнства и младенчества. 2025;2(1):79-85. https://doi.org/10.69964/BMCC-2025-2-1-79-85
For citation:
Zornikov D.L., Nechaeva D.M., Simarzina V.M., Kornilov D.O., Kariakina A.E., Amineva P.G., Voroshilina E.S. Impact of Chlorhexidine Digluconate on Bacterial DNA Preservation and PCR Efficiency. Bulletin of maternal and child care. 2025;2(1):79-85. (In Russ.) https://doi.org/10.69964/BMCC-2025-2-1-79-85
JATS XML









